Постановление Суда по интеллектуальным правам от 29 октября 2019 г. N С01-906/2019 по делу N А40-166505/2017 Судебные акты об удовлетворении иска о предоставлении принудительной простой (неисключительной) лицензии оставлены без изменения, поскольку суды признали согласно представленным в материалах дела доказательствам, что изобретение истца имеет существенные экономические преимущества по отношению к изобретению ответчика
Резолютивная часть постановления объявлена 24 октября 2019 года.
Полный текст постановления изготовлен 29 октября 2019 года.
Суд по интеллектуальным правам в составе:
председательствующего судьи Снегура А.А.,
судей Силаева Р.В., Четвертаковой Е.С.
рассмотрел в открытом судебном заседании кассационную жалобу иностранных лиц - Sugen LLC (230 East Grand Avenue South San Francisco, CA 94080 United States), PHARMACIA & UPJOHN COMPANY LLC (100 Route 206 North Peapack, NJ 07977 United States) и кассационную жалобу общества с ограниченной ответственностью "Натива" (ул. Октябрьская, д. 13, г. Красногорск, Московская область, 142402, ОГРН 1107746352163) на решение Арбитражного суда города Москвы от 08.02.2019 по делу N А40-166505/2017 и постановление Девятого апелляционного арбитражного суда от 07.05.2019 по тому же делу
по первоначальному иску иностранного лица - Sugen LLC и иностранного лица - PHARMACIA & UPJOHN COMPANY LLC к обществу с ограниченной ответственностью "Натива" и Министерству здравоохранения Российской Федерации (Рахмановский переулок, д. 3/25, стр. 1; 2; 3; 4, Москва, 127994, ОГРН 1127746460896) о защите исключительного права на изобретение,
по встречному иску общества с ограниченной ответственностью "Натива" к иностранным лицам Sugen LLC и PHARMACIA & UPJOHN COMPANY LLC о предоставлении принудительной простой (неисключительной) лицензии.
К участию в деле в качестве третьего лица, не заявляющего самостоятельных требований относительно предмета спора, привлечен Михайлов Олег Ростиславович (Москва).
В судебном заседании приняли участие представители:
от иностранного лица - Sugen LLC - Дякин Д.Б., Еременко В.Г., Родионов В.И., Рихтерман В.Я., Садовский П.В. (по совместной доверенности от 08.07.2019), Угрюмов В.М. (по доверенности от 15.02.2018);
от иностранного лица - PHARMACIA & UPJOHN COMPANY LLC - Угрюмов В.М. (по доверенности от 22.02.2017);
от общества с ограниченной ответственностью "Натива" - Герасимова Ю.П. (по доверенности от 09.04.2019 N 13) и Гусейнова У.А. (по доверенности от 06.06.2019 N 19).
Суд по интеллектуальным правам
УСТАНОВИЛ:
иностранные лица - Sugen LLC (далее - компания Sugen LLC) и PHARMACIA & UPJOHN COMPANY LLC (далее - компания PHARMACIA & UPJOHN COMPANY LLC) обратились в Арбитражный суд города Москвы с исковым заявлением к обществу с ограниченной ответственностью "Натива" (далее - общество) и Министерству здравоохранения Российской Федерации (Минздраву России) со следующими требованиями:
об обязании общества прекратить нарушения евразийского патента N 005996, в том числе запретить изготовление, предложение о продаже, продажу, иное введение в гражданский оборот и хранение для этих целей лекарственного препарата под любым торговым названием, содержащим вещество сунитиниб, в том числе в лекарственном препарате под торговым наименованием "Сунитиб-натив";
об обязании Минздрава России отменить государственную регистрацию лекарственного препарата "Сунитиниб-натив" (регистрационное удостоверение от 16.03.2017 N ЛП-004193) и исключить этот лекарственный препарат из государственного реестра лекарственных средств, отменить государственную регистрацию предельной отпускной цены на лекарственный препарат "Сунитиб-натив" от 19.05.2017 (274/20-17).
На основании статьи 51 Арбитражного процессуального кодекса Российской Федерации к участию в деле в качестве третьего лица, не заявляющего самостоятельных требований относительно предмета спора, привлечен Михайлов Олег Ростиславович.
В порядке, предусмотренном статьей 132 Арбитражного процессуального кодекса Российской Федерации, определением от 07.03.2018 Арбитражный суд города Москвы принял к производству встречные исковые требования общества следующего содержания:
о признании изобретения, охраняемого евразийским патентом N 005996, и изобретения, охраняемого патентом Российской Федерации N 2567535, зависимыми;
об обязании компаний Sugen LLC и PHARMACIA & UPJOHN COMPANY LLC предоставить принудительную простую (неисключительную) лицензию на использование на территории Российской Федерации изобретения, охраняемого евразийским патентом N 005996, на определенных условиях;
об обязании компаний Sugen LLC и PHARMACIA & UPJOHN COMPANY LLC зарегистрировать договор принудительной простой (неисключительной) лицензии на использование на территории Российской Федерации изобретения, охраняемого евразийским патентом N 005996, между обществом и названными компаниями.
Решением Арбитражного суда города Москвы от 08.02.2019 в удовлетворении первоначальных исковых требований отказано, встречные исковые требования удовлетворены.
Постановлением Девятого арбитражного апелляционного суда от 07.05.2019 решение Арбитражного суда города Москвы от 08.02.2019 оставлено без изменения.
Компании Sugen LLC и PHARMACIA & UPJOHN COMPANY LLC обратились в Суд по интеллектуальным правам с кассационной жалобой на указанные судебные акты.
Общество, не согласившись с принятыми по делу судебными актами, также обратилось в Суд по интеллектуальным правам с кассационной жалобой.
Компании Sugen LLC и PHARMACIA & UPJOHN COMPANY LLC, ссылаясь на нарушение судами первой и апелляционной инстанций норм материального и процессуального права, несоответствие выводов судов установленным фактическим обстоятельствам дела, просят отменить обжалуемые судебные акты и направить дело на новое рассмотрение.
По утверждению истцов по первоначальному иску, общество не использует изобретение по принадлежащему ему патенту Российской Федерации N 2567535 в лекарственном препарате "Сунитиниб-натив", а использует только изобретение истцов по евразийскому патенту N 005996, что исключает возможность удовлетворения иска о выдаче принудительной лицензии, так как она может предоставляться только в целях использования зависимого изобретения.
Как полагают компании Sugen LLC и PHARMACIA & UPJOHN COMPANY LLC, изобретение ответчика по первоначальному иску не представляет собой важное техническое достижение и не имеет существенных экономических преимуществ перед изобретением по патенту истцов по первоначальному иску, в связи с чем изобретение по патенту Российской Федерации N 2567535 не соответствует ни одному из критериев, установленных пунктом 2 статьи 1362 Гражданского кодекса Российской Федерации (далее - ГК РФ).
Истцы по первоначальному иску отмечают, что в целях правильной оценки экономических преимуществ суды должны были проанализировать влияние изобретений на себестоимость конкретных лекарственных препаратов, а также принимать во внимание все затраты на научные разработки.
Компании Sugen LLC и PHARMACIA & UPJOHN COMPANY LLC полагают, что установление стоимости лицензии в размере 10% от доходной части цены на лекарственный препарат общества не соответствует общепринятым условиям лицензирования при сравнимых обстоятельствах, данные платежи не смогут обеспечить получение хоть какой-то прибыли истцами по первоначальному иску.
Истцы по первоначальному иску обращают внимание на то, что на момент предъявления встречного иска истец по встречному иску не являлся правообладателем патента Российской Федерации N 2567535.
С точки зрения компаний Sugen LLC и PHARMACIA & UPJOHN COMPANY LLC, принудительное лицензирование может быть оправдано с позиции общественного интереса только в том случае, если в результате потребители получат конкретный препарат с улучшенными характеристиками.
Истцы по первоначальному иску считают, что вывод судов об использовании в лекарственном препарате общества изобретения по его патенту, основанный на ответах экспертов Лалаева Б.Ю. и Мус Г.П., не соответствует имеющимся в деле доказательствам, так как в действительности в лекарственном препарате общества изобретение по его патенту не используется, такой вывод мог быть сделан только в результате исследования образцов лекарственного препарата "Сунитиниб-натив".
По мнению компаний Sugen LLC и PHARMACIA & UPJOHN COMPANY LLC, патент общества защищает не само вещество сунитиниб, а лишь его специфическую кристаллическую модификацию, характеризующуюся определенным набором межплоскостных расстояний и соответствующих им интенсивностей.
В опровержение выводов вышеназванных судебных экспертов истцы по первоначальному иску ссылаются на представленное ими в материалы дела заключение специалиста Корлюкова А.А., согласно которому лекарственный препарат ответчика не содержит в качестве действующего вещества кристаллическую 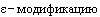 сунитиниба, характеризующуюся определенным набором межплоскостных расстояний (42 пика), а также соответствующих им интенсивностей и охраняемую патентом общества.
сунитиниба, характеризующуюся определенным набором межплоскостных расстояний (42 пика), а также соответствующих им интенсивностей и охраняемую патентом общества.
При этом, ссылаясь на норму части 5 статьи 69 Арбитражного процессуального кодекса Российской Федерации, истцы по первоначальному иску полагают, что суд первой инстанции не мог не принять выводы, изложенные в заключении специалиста Корлюкова А.А.
Также компании Sugen LLC и PHARMACIA & UPJOHN COMPANY LLC указывают на необоснованность отклонения судами отчета научной лаборатории, который был составлен по результатам спектрального анализа образцов лекарственного препарата общества и подтверждает, что он не содержит изобретение по патенту общества.
Истцы по первоначальному иску отмечают, что суды придали заранее установленную силу заключениям экспертов Лалаева Б.Ю. и Мус Г.П., несмотря на их очевидную научную необоснованность, а также многочисленные противоречия заключению эксперта Мошковского С.А. и иным доказательствам по делу.
По мнению компаний Sugen LLC и PHARMACIA & UPJOHN COMPANY LLC, инструкция по применению лекарственного препарата общества и опытно-промышленный регламент не могли быть положены в основу выводов экспертов, так как являются ненадлежащими объектами исследования.
С учетом этого истцы по первоначальному иску считают, что выводы экспертов Лалаева Б.Ю. и Мус Г.П. не соответствуют критерию проверяемости, ввиду чего их заключения не могли быть признаны судами достоверным доказательством по делу.
Исследованный экспертами опытно-промышленный регламент, с точки зрения компаний Sugen LLC и PHARMACIA & UPJOHN COMPANY LLC, является неотносимым доказательством, поскольку он описывает производство не промышленных партий, а лишь опытных образцов лекарственного препарата общества.
Истцы по первоначальному иску указывают на наличие у них сомнений в беспристрастности экспертов Лалаева Б.Ю. и Мус Г.П., поскольку указанные эксперты не исследовали имевшийся в материалах дела отчет научной лаборатории.
Компании Sugen LLC и PHARMACIA & UPJOHN COMPANY LLC обращают внимание на то, что в рамках проведенной по делу судебной экспертизы эксперты не смогли прийти к единому мнению по вопросу о том, является ли изобретение по патенту общества важным техническим достижением, так как, учитывая отсутствие легального определения понятия "важное техническое достижение", каждый эксперт исходил из своих собственных критериев оценки.
Вместе с тем истцы по первоначальному иску полагают, что зависимое изобретение в области фармацевтики, представляющее собой важное техническое достижение по сравнению с первым изобретением, может обеспечивать различные преимущества соответствующего лекарственного препарата с точки зрения фармакологии (то есть повышение эффективности, безопасности, уменьшение побочных эффектов и т.д.) или фармации (то есть увеличение сроков хранения, улучшение полезных характеристик при производстве и т.д.), однако соответствующие терапевтические преимущества лекарственного препарата, в котором используется зависимое изобретение, должны подтверждаться проведением полноценных клинических исследований.
Компании Sugen LLC и PHARMACIA & UPJOHN COMPANY LLC указывают на необоснованность выводов экспертов Лалаева Б.Ю. и Мус Г.П. о том, что факт выдачи патента на изобретение общества сам по себе является доказательством того, что данное изобретение представляет собой важное техническое достижение, и о том, что разница в скорости появления действующего вещества в крови кроликов подтверждает важность технического достижения изобретения по патенту общества.
Также, по мнению истцов по первоначальному иску, тот факт, что сунитиниб может демонстрировать полиформизм, не свидетельствует о том, что конкретная кристаллическая модификация сунитиниба имеет какие-либо технические преимущества.
Не соглашаясь с выводом судов о том, что зависимое изобретение общества имеет существенные экономические преимущества, компании Sugen LLC и PHARMACIA & UPJOHN COMPANY LLC акцентируют внимание на том, что суды необоснованно проигнорировали заключение судебного эксперта Мошковского С.А., который, основываясь на сравнении описаний патентов, пришел к выводу, что изобретение по патенту общества не имеет каких-либо экономических преимуществ перед изобретением по патенту истцов по первоначальному иску. При этом указанные заявители кассационной жалобы обращают внимание на то, что в материалах дела отсутствуют доказательства наличия существенных экономических преимуществ у изобретения по патенту общества.
Возражая против заключения заведующей сектором гражданского права Института государства и права Российской академии наук Санниковой Л.В., истцы по первоначальному иску заявляют, что содержащиеся в этом заключении выводы по экономическим проблемам принудительного лицензирования явно выходят за пределы ее компетенции и специализации в области правового режима цифровых активов, обязательств об оказании услуг, финансовых услуг и защиты прав потребителей.
Компании Sugen LLC и PHARMACIA & UPJOHN COMPANY LLC обращают внимание на то, что в патенте общества отсутствуют сведения, которые могли бы свидетельствовать о наличии экономической эффективности основанного на этом изобретении препарата.
Как полагают истцы по первоначальному иску, для проведения судебной экспертизы по вопросу о наличии существенных экономических преимуществ суды должны были привлечь экспертов, обладающих необходимыми знаниями в этой области.
Компании Sugen LLC и PHARMACIA & UPJOHN COMPANY LLC настаивают на том, что вычисление какого-либо процента от доходной части цены на производимый на основании лицензии лекарственный препарат не является общепринятым и обоснованным способом расчета лицензионных платежей в фармацевтической промышленности.
По мнению истцов по первоначальному иску, в нарушение пункта 2 статьи 1362 ГК РФ суды обязали их выдать обществу принудительную лицензию на использование сунитиниба во всех его формах, а не только на кристаллическую модификацию, охраняемую патентом общества.
Компании Sugen LLC и PHARMACIA & UPJOHN COMPANY LLC считают, что суды первой и апелляционной инстанций необоснованно отклонили их ходатайства о назначении повторной судебной экспертизы, а также заявления об отводах судебных экспертов Лалаева Б.Ю. и Мус Г.П.
Кроме того, истцы по первоначальному иску отмечают, что резолютивная часть решения суда первой инстанции не соответствует заявленным обществом требованиям по встречному иску.
С точки зрения компаний Sugen LLC и PHARMACIA & UPJOHN COMPANY LLC, обжалуемые судебные акты приняты об обязанностях Федеральной службы по интеллектуальной собственности (Роспатента), не привлеченной к участию в деле, так как предписание суда обязать ответчиков по встречному иску в установленном законом порядке зарегистрировать договор принудительной простой (неисключительной) лицензии подразумевает обязанность Роспатента зарегистрировать такую принудительную лицензию.
Компанией Sugen LLC 30.09.2019 было представлено дополнение к кассационной жалобе, в котором он ссылается на позицию Роспатента, изложенную в письме от 10.07.2019.
Указанная компания также обращает внимание на то, что заключение эксперта Мус Г.П. аналогично заключению эксперта Семенова В.И., составленному в рамках дела N А40-71471/2017, что, по ее мнению, ставит под сомнение научную обоснованность выводов эксперта Мус Г.П.
Компания Sugen LLC отмечает, что суды, не обладая специальными познаниями и не назначив повторную либо дополнительную экспертизу, самостоятельно разрешили возникшие между экспертами противоречия.
Общество в поданной в Суд по интеллектуальным правам кассационной жалобе просит изменить обжалуемые решение и постановление в части удовлетворения требования по встречному иску об обязании компаний Sugen LLC и PHARMACIA & UPJOHN COMPANY LLC в установленном законом порядке зарегистрировать договор принудительной простой (неисключительной) лицензии на использование на территории Российской Федерации изобретения под названием "Пирролзамещенный 2-индолинон, фармацевтическая композиция (варианты), способ модулирования каталитической активности протеинкиназы, способ лечения или профилактики нарушения в организме, связанного с протеинкиназой", охраняемого евразийским патентом N 005996, между обществом и компаниями Sugen LLC и PHARMACIA & UPJOHN COMPANY LLC и удовлетворить требования по встречному иску, обязав компании Sugen LLC и PHARMACIA & UPJOHN COMPANY LLC совершить необходимые действия, предусмотренные действующим законодательством для осуществления государственной регистрации договора принудительной простой (неисключительной) лицензии на использование на территории Российской Федерации вышеназванного изобретения между обществом и компаниями Sugen LLC и PHARMACIA & UPJOHN COMPANY LLC.
Общество считает, что судами неверно истолкованы нормы, закрепленные в статьях 1232 и 1235 ГК РФ, согласно которым функции по регистрации перехода права пользования по лицензионному договору возлагаются на соответствующий орган исполнительной власти (Роспатент), а стороны должны предпринять ряд действий, необходимых для осуществления такой регистрации.
Компаниями Sugen LLC и PHARMACIA & UPJOHN COMPANY LLC представлен отзыв на кассационную жалобу общества, в котором они просят отказать в удовлетворении этой жалобы, поскольку исковое требование истца по встречному иску "совершить необходимые действия для осуществления государственной регистрации договора" не содержалось во встречном исковом заявлении и было фактически предъявлено только в апелляционной жалобе общества на решение суда первой инстанции.
Обществом представлен отзыв на кассационную жалобу компаний Sugen LLC и PHARMACIA & UPJOHN COMPANY LLC, в котором оно возражает против изложенных в ней доводов.
Как полагает общество, судами в полном объеме были исследованы все доказательства, подтверждающие использование патента Российской Федерации N 2567535 обществом при производстве лекарственного препарата "Сунитиниб-натив".
Общество указывает на то, что обязательность наличия промышленного регламента предусмотрена нормативными правовыми актами и на любом предприятии фармацевтической промышленности производство лекарственных средств должно осуществляться на основании промышленного регламента.
Возражая против довода компаний Sugen LLC и PHARMACIA & UPJOHN COMPANY LLC о том, что общество не могло обращаться со встречным исковым заявлением, так как не являлось обладателем патента Российской Федерации N 2567535, общество отмечает, что на момент принятия встречного искового заявления между обществом и Михайловым О.Р. был заключен договор об отчуждении исключительного права от 09.02.2018 N 1C, переход прав по которому был зарегистрирован Роспатентом 23.03.2018. Также общество указывает, что после получения письменного подтверждения о регистрации перехода права общество сделало заявление о процессуальном правопреемстве, которое было удовлетворено судом первой инстанции.
По мнению общества, доводы компаний Sugen LLC и PHARMACIA & UPJOHN COMPANY LLC по сути сводятся к несогласию с результатами судебной экспертизы и их толкованию судами первой и апелляционной инстанций.
При этом общество полагает, что выводы эксперта Мошковского С.А. были основаны на предположениях, эксперт подменил понятие "большая биологическая доступность" понятием "биоэквивалентность".
Как полагает общество, истцы по первоначальному иску ошибочно считают, что при решении вопроса о предоставлении принудительной лицензии подлежат сравнению лекарственные средства, тогда как должны сравниваться два изобретения.
Общество утверждает, что уточняло исковые требования, которые были сформулированы именно так, как суд первой инстанции указал в резолютивной части решения.
Компаниями Sugen LLC и PHARMACIA & UPJOHN COMPANY LLC 22.10.2019 представлены письменные возражения на отзыв общества на кассационную жалобу.
Минздравом России отзывы на кассационные жалобы не представлены.
В судебном заседании 01.10.2019 на основании части 2 статьи 287 Арбитражного процессуального кодекса Российской Федерации возвращены приложенные к кассационной жалобе компаний Sugen LLC и PHARMACIA & UPJOHN COMPANY LLC и к дополнению компании Sugen LLC к указанной кассационной жалобе дополнительные доказательства, которые не представлялись при рассмотрении дела в судах первой и апелляционной инстанций. Представители компаний Sugen LLC и PHARMACIA & UPJOHN COMPANY LLC в этом судебном заседании выступили по доводам, изложенным в кассационной жалобе, дополнении к ней.
Определением Суда по интеллектуальным правам от 01.10.2019 судебное заседание по рассмотрению кассационных жалоб было отложено на 24.10.2019 в связи с поступлением непосредственно перед судебным заседанием дополнительных процессуальных документов.
В судебном заседании 24.10.2019 представители общества поддержали доводы, изложенные в кассационной жалобе общества и отзыве на кассационную жалобу компаний Sugen LLC и PHARMACIA & UPJOHN COMPANY LLC.
Представители компаний Sugen LLC и PHARMACIA & UPJOHN COMPANY LLC возражали против удовлетворения кассационной жалобы общества, а также выступили по доводам, изложенным в письменных возражениях на отзыв общества.
Минздрав России и Михайлов О.Р., извещенные надлежащим образом о времени и месте рассмотрения кассационных жалоб, в судебное заседание не явились, явку представителей не обеспечили, что в силу части 3 статьи 284 Арбитражного процессуального кодекса Российской Федерации не является препятствием для рассмотрения дела в их отсутствие.
Согласно правовой позиции, изложенной в пункте 5 постановления Пленума Высшего Арбитражного Суда Российской Федерации от 17.02.2011 N 12 "О некоторых вопросах применения Арбитражного процессуального кодекса Российской Федерации в редакции Федерального закона от 27.07.2010 N 228-ФЗ "О внесении изменений в Арбитражный процессуальный кодекс Российской Федерации", при наличии в материалах дела уведомления о вручении лицу, участвующему в деле, либо иному участнику арбитражного процесса копии первого судебного акта по рассматриваемому делу либо сведений, указанных в части 4 статьи 123 Арбитражного процессуального кодекса Российской Федерации, такое лицо считается надлежаще извещенным при рассмотрении дела судом апелляционной, кассационной, надзорной инстанции, при рассмотрении судом первой инстанции заявления по вопросу о судебных расходах, если судом, рассматривающим дело, выполняются обязанности по размещению информации о времени и месте судебных заседаний, совершении отдельных процессуальных действий на официальном сайте арбитражного суда в сети Интернет в соответствии с требованиями абзаца второго части 1 статьи 121 Арбитражного процессуального кодекса Российской Федерации. При этом отсутствие в материалах дела доказательств, подтверждающих получение лицами, участвующими в деле, названных документов, не может расцениваться как несоблюдение арбитражным судом правил Арбитражного процессуального кодекса Российской Федерации о надлежащем извещении.
Законность обжалуемых судебных актов проверена арбитражным судом кассационной инстанции в порядке, предусмотренном статьями 284 и 286 Арбитражного процессуального кодекса Российской Федерации, исходя из доводов, содержащихся в кассационных жалобах, дополнении к кассационной жалобе, отзывах на кассационные жалобы и письменных возражениях.
Как следует из материалов дела и установлено судами первой и апелляционной инстанций, компании Sugen LLC и PHARMACIA & UPJOHN COMPANY LLC, входящие в группу компаний Пфайзер, являются разработчиками противоопухолевого лекарственного средства с действующим веществом сунитиниб в соответствии с международным непатентованным наименованием (МНН), поставляемого на российский рынок компанией Пфайзер под торговым названием "Сутент" (регистрационное удостоверение от 31.08.2007 N ЛСР002516/07).
Указанные лица являются обладателями действующего на территории Российской Федерации евразийского патента N 005996 на изобретение "Пирролзамещенный 2-индолинон, фармацевтическая композиция (варианты), способ модулирования каталитической активности протеинкиназы, способ лечения или профилактики нарушения в организме, связанного с протеинкиназой" с приоритетом от 15.02.2000, зарегистрированного 25.08.2005. Срок действия указанного патента в отношении пунктов 1, 10 и 12 формулы изобретения продлен до 31.08.2022.
По мнению истцов по первоначальному иску, принадлежащее им исключительное право на изобретение по евразийскому патенту N 005996 было нарушено путем несанкционированного введения в обращение лекарственного препарата под торговым наименованием "Сунитиниб-натив", производителем которого является общество, и который является воспроизведенным препаратом (дженериком) по отношению к референтному (оригинальному) препарату "Сутент", также содержащим в качестве действующего вещества сунитиниб.
Компании Sugen LLC и PHARMACIA & UPJOHN COMPANY LLC согласия на использование изобретения по евразийскому патенту N 005996 обществу не давали, самостоятельно используют запатентованное изобретение путем введения в обращение с 2007 года референтного лекарственного препарата под названием "Сутент", содержащего сунитиниб в качестве действующего вещества.
На основании документов, представленных обществом, и проведенных экспертиз качества лекарственного средства и ожидаемой пользы от возможного применения лекарственного препарата Минздрав России принял решение о государственной регистрации лекарственного препарата под торговым наименованием "Сунитиниб-натив" (регистрационное удостоверение от 16.03.2017 N ЛП-004193).
Кроме того, Минздравом России 19.05.2017 было принято решение о государственной регистрации предельной отпускной цены на препарат Сунитиниб-натив (N 274/20-17), о чем были внесены соответствующие данные в государственный реестр предельных отпускных цен.
Исходя из изложенного, компании Sugen LLC и PHARMACIA & UPJOHN COMPANY LLC обратились в суд с первоначальным иском к обществу и Минздраву России.
Заявляя встречный иск, общество указало на то, что является производителем лекарственного препарата "Сунитиниб-натив", содержащего в качестве активного вещества сунитиниб, сведения о котором содержатся в государственном реестре лекарственных средств.
При этом, по утверждению общества, при производстве лекарственного препарата "Сунитиниб-натив" оно использует собственное изобретение, охраняемое патентом Российской Федерации N 2567535, указанное изобретение является зависимым по отношению к изобретению, охраняемому евразийским патентом N 005996 в понимании статьи 1358.1 ГК РФ.
Общество полагает, что не имеет возможности использовать свое изобретение по патенту Российской Федерации N 2567535 без использования изобретения по евразийскому патенту N 005996 с более ранней датой приоритета.
В январе 2018 года общество обратилось к компании Sugen LLC с предложением заключить лицензионный договор на использование исключительного права на изобретение, охраняемое евразийским патентом N 005996, предложив следующие условия: срок лицензии - до 30.08.2022 года; территория действия лицензионного договора - Российская Федерация; способ использования изобретения - изготовление, применение, предложение к продаже, продажа и хранение для этих целей продукции, при изготовлении которой используется изобретение по евразийскому патенту N 005996; вознаграждение за использование изобретения - 10% доходности от продажи лекарственных препаратов с МНН "Сунитиниб" (производства общества) на территории Российской Федерации. На указанное предложение положительный ответ от правообладателей евразийского патента N 005996 получен не был.
По утверждению истца по встречному иску, изобретение, охраняемое патентом Российской Федерации N 2567535 (которое используется обществом), представляет собой важное техническое достижение и имеет существенные экономические преимущества перед изобретением, охраняемым евразийским патентом N 005996.
Лекарственные препараты с МНН "Сунитиниб" входят в перечень жизненно необходимых и важнейших лекарственных препаратов на 2017 и 2018 годы (распоряжения Правительства Российской Федерации от 28.12.2016 N 2885-р и от 23.10.2017 N 2323-р соответственно).
Судами первой и апелляционной инстанции установлено, что и на лекарственный препарат "Сутент", и на лекарственный препарат "Сунитиниб-натив" зарегистрированы предельные отпускные цены, сведения о которых являются публичными и содержатся в государственном реестре предельных отпускных цен.
В ходе судебного разбирательства сторонами были заявлены ходатайства о назначении комплексной патентно-технической судебной экспертизы. Принимая во внимание необходимость наличия специальных познаний для разрешения поставленных сторонами вопросов, суд первой инстанции определением от 01.06.2018 назначил по делу комплексную судебную патентно-техническую экспертизу по вопросам, требующим специальных знаний в области химии, фармакологии, медицины, патентоведения, а именно:
1. Является ли изобретение, охраняемое Российской Федерации патентом N 2567535, под названием "Кристаллическая 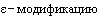 К-[2-(диэтиламино)этил]-5-[(г)-(5-фтор-1,2-дигидро-2-оксо-ЗН-индол-3-илиден)метил]-2,4-диметил-1Н-пиррол-3-карбоксамид малата, способ ее получения и фармацевтическая композиция на ее основе" зависимым по отношению к изобретению, охраняемому евразийским патентом N 005996, под названием "Пирролзамещенный 2-индолинон, фармацевтическая композиция (варианты), способ модулирования каталитической активности протеинкиназы, способ лечения или профилактики нарушения в организме, связанного с протеинкиназой"?
К-[2-(диэтиламино)этил]-5-[(г)-(5-фтор-1,2-дигидро-2-оксо-ЗН-индол-3-илиден)метил]-2,4-диметил-1Н-пиррол-3-карбоксамид малата, способ ее получения и фармацевтическая композиция на ее основе" зависимым по отношению к изобретению, охраняемому евразийским патентом N 005996, под названием "Пирролзамещенный 2-индолинон, фармацевтическая композиция (варианты), способ модулирования каталитической активности протеинкиназы, способ лечения или профилактики нарушения в организме, связанного с протеинкиназой"?
2. Используется ли изобретение, охраняемое патентом Российской Федерации N 2567535, под названием "Кристаллическая 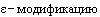 Н-[2-(диэтиламино)этил]-5-[(/)-(5-фтор-1,2-дигидро-2-оксо-ЗН-индол-3-илиден)метил]-2,4-диметил-1Н-пиррол-3-карбоксамид маната, способ ее получения и фармацевтическая композиция на ее основе" в фармацевтической субстанции "Сунитиниб" (производитель общество), реестровая запись ФС 001601-300117 в государственном реестре лекарственных средств, и в лекарственном препарате "Сунитиниб-натив", регистрационное удостоверение от 16.03.2017 N ЛП-004193?
Н-[2-(диэтиламино)этил]-5-[(/)-(5-фтор-1,2-дигидро-2-оксо-ЗН-индол-3-илиден)метил]-2,4-диметил-1Н-пиррол-3-карбоксамид маната, способ ее получения и фармацевтическая композиция на ее основе" в фармацевтической субстанции "Сунитиниб" (производитель общество), реестровая запись ФС 001601-300117 в государственном реестре лекарственных средств, и в лекарственном препарате "Сунитиниб-натив", регистрационное удостоверение от 16.03.2017 N ЛП-004193?
3. Является ли изобретение, охраняемое патентом Российской Федерации N 2567535, под названием "Кристаллическая 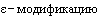 N-[2-(диэтиламино)этил]-5-[(7)-(5-фтор-1,2-дигидро-2-оксо-ЗН-индол-3-илиден)метил]-2,4-диметил-1Н-пиррол-3-карбоксамид малата, способ ее получения и фармацевтическая композиция на ее основе", срок начала действия патента 01.10.2014, важным техническим достижением по отношению к изобретению, охраняемому евразийским патентом N 005996, под названием "Пирролзамещенный 2-индолинон, фармацевтическая композиция (варианты), способ модулирования каталитической активности протеинкиназы, способ лечения или профилактики нарушения в организме, связанного с протеинкиназой", срок начала действия патента 12.04.2000?
N-[2-(диэтиламино)этил]-5-[(7)-(5-фтор-1,2-дигидро-2-оксо-ЗН-индол-3-илиден)метил]-2,4-диметил-1Н-пиррол-3-карбоксамид малата, способ ее получения и фармацевтическая композиция на ее основе", срок начала действия патента 01.10.2014, важным техническим достижением по отношению к изобретению, охраняемому евразийским патентом N 005996, под названием "Пирролзамещенный 2-индолинон, фармацевтическая композиция (варианты), способ модулирования каталитической активности протеинкиназы, способ лечения или профилактики нарушения в организме, связанного с протеинкиназой", срок начала действия патента 12.04.2000?
4. Имеет ли изобретение, охраняемое патентом Российской Федерации N 2567535, под названием "Кристаллическая 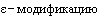 N-[2-(диэтиламино)этил]-5-[(7)-(5-фтор-1,2-дигидро-2-оксо-ЗН-индол-3-илиден)метил]-2,4-диметил-1Н-пиррол-3-карбоксамид малата, способ ее получения и фармацевтическая композиция на ее основе", срок начала действия патента 01.10.2014, существенные экономические преимущества по отношению к изобретению, охраняемому евразийским патентом N 005996, под названием "пирролзамещенный 2-индолинон, фармацевтическая композиция (варианты), способ модулирования каталитической активности протеинкиназы, способ лечения или профилактики нарушения в организме, связанного с протеинкиназой", срок начала действия патента 12.04.2000?
N-[2-(диэтиламино)этил]-5-[(7)-(5-фтор-1,2-дигидро-2-оксо-ЗН-индол-3-илиден)метил]-2,4-диметил-1Н-пиррол-3-карбоксамид малата, способ ее получения и фармацевтическая композиция на ее основе", срок начала действия патента 01.10.2014, существенные экономические преимущества по отношению к изобретению, охраняемому евразийским патентом N 005996, под названием "пирролзамещенный 2-индолинон, фармацевтическая композиция (варианты), способ модулирования каталитической активности протеинкиназы, способ лечения или профилактики нарушения в организме, связанного с протеинкиназой", срок начала действия патента 12.04.2000?
В представленном в материалы дела экспертном заключении по результатам комплексной патентно-технической судебной экспертизы эксперты Мус Г.П., Лалаев Б.Ю. и Мошковский С.А. совместно подтвердили, что изобретение охраняемое патентом Российской Федерации N 2567535 от 01.10.2014, под названием "Кристаллическая 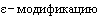 К-[2-(диэтиламино)этил]-5-[(г)-(5-фтор1,2-дигидро-2-оксо-ЗН-индол-3-илиден)метил]-2,4-диметил-1Н-пиррол-3-карбоксамид малата, способ ее получения и фармацевтическая композиция на ее основе" является зависимым по отношению к изобретению, охраняемому евразийским патентом N 005996, под названием "Пирролзамещенный 2-индолинон, фармацевтическая композиция (варианты), способ модулирования каталитической активности протеинкиназы, способ лечения или профилактики нарушения в организме, связанного с протеинкиназой".
К-[2-(диэтиламино)этил]-5-[(г)-(5-фтор1,2-дигидро-2-оксо-ЗН-индол-3-илиден)метил]-2,4-диметил-1Н-пиррол-3-карбоксамид малата, способ ее получения и фармацевтическая композиция на ее основе" является зависимым по отношению к изобретению, охраняемому евразийским патентом N 005996, под названием "Пирролзамещенный 2-индолинон, фармацевтическая композиция (варианты), способ модулирования каталитической активности протеинкиназы, способ лечения или профилактики нарушения в организме, связанного с протеинкиназой".
Эксперты Мус Г.П. и Лалаев Б.Ю. установили, что изобретение, охраняемое патентом Российской Федерации N 2567535, используется в фармацевтической субстанции "Сунитиниб" и в лекарственном препарате "Сунитиниб-натив". Также указанными экспертами было установлено, что изобретение, охраняемое патентом Российской Федерации N 2567535, является важным техническим достижением. Между тем, выводы эксперта Мошковского С.А. по указанным вопросам были отрицательными.
Отвечая на четвертый вопрос, эксперт Мус Г.П. указала, что в отсутствии необходимой экономической квалификации затрудняется предоставить надлежащий вывод. Эксперт Лалаев Б.Ю. при ответе на четвертый вопрос подтвердил, что изобретение, охраняемое патентом Российской Федерации N 2567535, имеет существенные экономические преимущества по отношению к изобретению, охраняемому евразийским патентом N 005996. В заключении эксперта Мошковского С.А. по четвертому вопросу сделан отрицательный вывод.
Суд первой инстанции, рассмотрев предоставленные доказательства, в том числе заключение комплексной судебной патентно-технической экспертизы в совокупности и взаимной связи, пришел к выводу об обоснованности требований, изложенных во встречном иске, и об отсутствии оснований для удовлетворения первоначального иска. При этом суд первой инстанции исходил из следующего.
Использование зависимого изобретения всегда будет нарушать права обладателя патента на основное изобретение, следовательно, на законной основе патентообладатель не может использовать изобретение.
Суд первой инстанции пришел к выводу о том, что изобретение по патенту Российской Федерации N 2567535 представляет собой важное техническое решение, основываясь, в том числе на заключении экспертов Мус. Г.П. и Лалаева Б.Ю.
Судом первой инстанции было установлено, что и изобретение общества, и изобретение, исключительным правом на которое обладают истцы по первоначальному иску, используется при изготовлении лекарственных препаратов для лечения тяжелых, в том числе, онкологических заболеваний. Разнообразие, которое позволит применить индивидуальный подход к лечению того или иного заболевания у людей, доступность лекарственных средств, а главное, эффективность ввиду важности технического решения, могут способствовать продлению, а также спасению жизни человека, что социально значимо для общества и государства.
Судом первой инстанции учтено, что истцы по первоначальному иску, отказываясь предоставлять лицензию без каких-либо обоснований, препятствуют и запрещают использовать изобретение по патенту Российской Федерации N 2567535.
Суд первой инстанции, проанализировав нормативные правовые акты, регулирующие производство лекарственных препаратов на основе промышленных регламентов, приняв во внимание, что любое отклонение в составе вещества препарата и его несоответствие, том числе заявленным характеристикам, виду и составу действующего вещества, указанному в промышленном регламенте, влечет для производителя соответствующую ответственность, в том числе уголовную, пришел к выводу о возможности использования промышленного регламента в качестве доказательства, позволяющего установить факт использования изобретения в лекарственном препарате.
Отклоняя ссылку истца по первоначальному иску на отчет научной лаборатории об исследовании образца лекарственного препарата "Сунитиниб-натив", суд первой инстанции исходил из того, что указанное исследование проведено за пределами Российской Федерации, по неизвестному препарату, с неизвестными условиями хранения, транспортировки, на неизвестном оборудовании, с использованием неустановленных методов исследования, в связи с чем признал данный отчет недопустимым доказательством. Также судом первой инстанции были приняты во внимание сроки проведения исследования, а именно то, что 04.05.2018 нотариус города Москвы Миллер Н.Н. произвел осмотр лекарственного препарата "Сунитиниб-натив" в натуре с целью обеспечения доказательств, а уже 07.05.2018 лаборатория Пфайзер, расположенная в городе Гротон, штат Коннектикут, США, сделала исследования и составила отчет, что является технически затруднительным.
Суд первой инстанции признал доводы истцов по первоначальному иску и вывод эксперта Мошковского С.А. о том, что инструкция по медицинскому применению не содержит сведения о кристаллической модификации противоречащими требованиям приказа Минздрава России от 21.09.2016 N 724н "Об утверждении требований к инструкции по медицинскому применению лекарственных препаратов".
Отклоняя доводы ответчиков по встречному иску, касающиеся правовых аспектов наличия оснований для предоставления простой принудительной лицензии, в частности о неприменимости норм действующего законодательства Российской Федерации в указанной части к фармацевтическим продуктам и их явном противоречии общемировой практике использования института принудительного лицензирования, суд первой инстанции указал, что согласно заключению заведующего сектором гражданского права Института государства и права Российской академии наук Санниковой Л.В. практика выдачи принудительных лицензий распространена не только в развивающихся странах (преимущественно на фармацевтические препараты, в том числе лекарства от онкологических заболеваний), но и в странах со средним уровнем дохода и ведущих развитых странах мира; при толковании словосочетания "важное техническое достижение" акцент следует делать не на слова "техническое достижение", так как любое запатентованное изобретение является техническим достижением, а на слово "важное"; зависимое изобретение должно содержать в себе такую инновацию, использование которой имеет важное значение для всего общества; при оценке зависимого изобретения с точки зрения важности необходимо учитывать значение предлагаемого технического решения для удовлетворения общественных интересов; для того, чтобы выявить экономическое преимущество, необходимо сравнить экономические показатели зависимого изобретения и того изобретения, которое было использовано в зависимом; выбор тех или иных экономических показателей для проведения такого сравнительного анализа зависит непосредственно от сущности самого изобретения; если в качестве зависимого изобретения выступает воспроизведенный лекарственный препарат, то есть основания предполагать, что его стоимость будет существенно ниже, чем у оригинального препарата.
Суд первой инстанции установил, что первоначальная предельная отпускная цена на препарат истца по встречному иску меньше как минимум на 20% относительно цены препарата истцов по первоначальному иску, а при проведении торгов разница в цене препаратов может достигнуть 60% и с учетом годового объема только государственных закупок согласно расчету истца по встречному иску годовая экономия бюджетных средств только по одному спорному препарату превысит 200 000 000 руб.
Исходя из этого, суд первой инстанции отметил, что наличие существенного экономического преимущества подтверждается не только заключением эксперта Лалаева Б.Ю., но и совокупностью представленных в материалы дела доказательств.
Установив наличие всех условий, предусмотренных статьей 1362 ГК РФ, суд первой инстанции пришел к выводу о наличии оснований для принятия решения о предоставлении принудительной простой (неисключительной) лицензии на использование на территории Российской Федерации изобретения, охраняемого патентом ответчиков по встречному иску.
Судом первой инстанции было отклонено ходатайство компаний Sugen LLC и PHARMACIA & UPJOHN COMPANY LLC о назначении по делу повторной судебной экспертизы ввиду отсутствия оснований, предусмотренных статьей 87 Арбитражного процессуального кодекса Российской Федерации для его удовлетворения, поскольку оно обусловлено исключительно несогласием истцов по первоначальному иску с результатами комплексной патентно-технической экспертизы, проведенной в рамках судебного разбирательства.
Не приняты судом первой инстанции по основаниям, аналогичным изложенным выше применительно к отчету научной лаборатории об исследовании образца лекарственного препарата "Сунитиниб-натив", и ссылки истцов по первоначальному иску на проведение во внесудебном порядке при участии нотариуса дополнительного исследования специалистом Корлюковым А.А. При этом суд первой инстанции отметил, что никакие доказательства не имеют для арбитражного суда заранее установленной силы, но заключение судебной экспертизы занимает среди них особое место при оценке его в ряде других доказательств, что объясняется тем, что суд в этом случае исследует такие факты, сведения о которых могут быть получены только в результате специального исследования - экспертизы, то есть эти факты могут быть подтверждены (или опровергнуты) лишь специальными познаниями в области науки, искусства, техники, строительства, информатизации и т.д., в связи с чем судебная экспертиза с привлечением специалистов имеющих специальные познания в отношении соответствующего направления развития науки и техники является важнейшим средством получения верного знания о факте (фактах).
Суд первой инстанции, оценив заключение комплексной судебной патентно-технической экспертизы в совокупности с представленными в материалы дела доказательствами в порядке, предусмотренном статьей 71 Арбитражного процессуального кодекса Российской Федерации, пришел к выводу о том, что представленное заключение экспертизы является достаточно ясным и полным, в нем содержатся ответы на поставленные судом перед экспертами вопросы со ссылкой на документы, которыми эксперты руководствовались, противоречивые доказательства в материалах дела отсутствуют, в связи с чем процессуальных оснований для назначения повторной экспертизы не имеется.
Суд первой инстанции в обжалуемом решении указал, что оснований для удовлетворения требований истцов по первоначальному иску к ответчику - Минздраву России также не имеется, поскольку доказательств нарушения указанным ответчиком процедуры регистрации лекарственного препарата ответчика по первоначальному иску не представлено, а удовлетворение встречных исковых требований по изложенным выше основаниям исключает возникновение у Минздрава России обязанности отменить государственную регистрацию лекарственного препарата (регистрационное удостоверение от 16.03.2017 N ЛП-004193) и исключить его из государственного реестра лекарственных средств, а также отменить государственную регистрацию предельной отпускной цены на лекарственный препарат "Сунитиниб-натив" от 19.05.2017 (274/20-17).
При этом суд первой инстанции отметил, что законодательством Российской Федерации об обращении лекарственных средств не предусматривается представление заявителем в Минздрав России в составе комплектов документов, подаваемых для целей государственной регистрации лекарственного препарата для медицинского применения, государственной регистрации устанавливаемых производителями лекарственных препаратов предельных отпускных цен на лекарственные препараты, документов и данных о наличии права интеллектуальной собственности на заявляемый лекарственный препарат; регистрация лекарственного препарата сама по себе не свидетельствует об использовании изобретения, воплощенного в лекарственном препарате, по смыслу статьи 1358 ГК РФ и не является нарушением исключительного права; исчерпывающий перечень оснований для отмены государственной регистрации лекарственного препарата и исключения из государственного реестра для медицинского применения установлен статьей 31 Федерального закона от 12.04.2010 N 61-ФЗ "Об обращении лекарственных средств" (далее - Закон об обращении лекарственных средств), какое-либо из предусмотренных в ней оснований в рассматриваемом случае судом не установлено.
Суд апелляционной инстанции поддержал выводы, содержащиеся в обжалуемом решении суда первой инстанции, отказав в удовлетворении апелляционных жалоб как компаний Sugen LLC и PHARMACIA & UPJOHN COMPANY LLC, так и общества.
Суд апелляционной инстанции отклонил доводы апелляционной жалобы компаний Sugen LLC и PHARMACIA & UPJOHN COMPANY LLC относительно необходимости проведения повторной экспертизы, поскольку указанные в обоснование данного довода обстоятельства не свидетельствуют о наличии оснований для проведения повторной экспертизы, а лишь выражают несогласие ответчика с результатами судебной экспертизы, в связи с чем в удовлетворении заявленного указанными лицами аналогичного ходатайства также было отказано.
Судом апелляционной инстанции не были приняты ссылки истцов по первоначальному иску относительно неполноты заключения судебной экспертизы, так как представленное в материалы дела заключение судебной экспертизы соответствует требованиям, предъявляемым к экспертным заключениям, не содержит противоречий и является полным исходя из поставленных судом первой инстанции перед экспертами вопросов.
Суд апелляционной инстанции отметил, что суд первой инстанции, приходя к выводу о наличии совокупности условий в соответствии с пунктом 2 статьи 1362 ГК РФ и оснований для удовлетворения встречных исковых требований, обоснованно оценил экспертное заключение наравне с другими доказательствами по делу, учел то, что изобретения истца и ответчика используются при изготовлении лекарственных препаратов для лечения тяжелых, в том числе, онкологических заболеваний, а обеспечение своевременного и качественного оказания специализированной медицинской помощи онкологическим больным является приоритетным для удовлетворения общественных интересов, однако истцы по первоначальному иску по факту отказываются предоставлять лицензию без каких-либо обоснований, препятствуют и запрещают использовать изобретение по патенту Российской Федерации N 2567535.
Суд апелляционной инстанции пришел к выводу о том, что, вопреки соответствующему доводу истцов по первоначальному иску, суд первой инстанции правильно применил нормы материального и процессуального права, дал надлежащую правовую оценку указанным в пункте 2 статьи 1362 ГК РФ признакам, необходимым для выдачи в принудительном порядке лицензии.
Судом апелляционной инстанции были отклонены доводы ответчиков по встречному иску относительно несоблюдения обществом претензионного порядка урегулирования спора и злоупотребления правом со стороны общества.
Отказывая в удовлетворении апелляционной жалобы общества, суд апелляционной инстанции исходил из того, что исковое требование обязать ответчиков по встречному иску "совершить необходимые действия для осуществления государственной регистрации договора" во встречном исковом заявлении отсутствовало, правом на изменение предмета встречного иска общество не воспользовалось, а у суда отсутствует право принимать решение по требованию, которое не было заявлено.
Изучив материалы дела, рассмотрев доводы, изложенные в кассационных жалобах, отзывах на них, письменных объяснениях, заслушав мнение представителей сторон, проверив в соответствии со статьями 286 и 287 Арбитражного процессуального кодекса Российской Федерации правильность применения судами первой и апелляционной инстанций норм материального и процессуального права, соответствие выводов судов имеющимся в деле доказательствам и установленным фактическим обстоятельствам, Суд по интеллектуальным правам не усматривает достаточных оснований для отмены (изменения) обжалуемых судебных актов.
Согласно пункту 1 статьи 1358 ГК РФ патентообладателю принадлежит исключительное право использования изобретения в соответствии со статьей 1229 этого Кодекса любым не противоречащим закону способом (исключительное право на изобретение), в том числе способами, предусмотренными пунктом 2 названной статьи.
Использованием изобретения считается, в частности, изготовление, применение, предложение о продаже, продажа, иное введение в гражданский оборот или хранение для этих целей продукта, в котором использованы изобретение или полезная модель, либо изделия, в котором использован промышленный образец (подпункт 1 пункта 2 статьи 1358 ГК РФ).
Пунктом 3 статьи 1358 ГК РФ предусмотрено, что изобретение признается использованным в продукте или способе, если продукт содержит, а в способе использован каждый признак изобретения, приведенный в независимом пункте содержащейся в патенте формулы изобретения, либо признак, эквивалентный ему и ставший известным в качестве такового в данной области техники до даты приоритета изобретения.
В силу пункта 1 статьи 1358.1 ГК РФ изобретение, полезная модель, промышленный образец, использование которых в продукте или способе невозможно без использования охраняемых патентом и имеющих более ранний приоритет другого изобретения, другой полезной модели или другого промышленного образца, соответственно являются зависимым изобретением, зависимой полезной моделью, зависимым промышленным образцом.
Судебной экспертизой установлено и сторонами не оспаривается тот факт, что изобретение по патенту Российской Федерации N 2567535, исключительное право на которое принадлежит обществу, является зависимым по отношению к изобретению по евразийскому патенту N 005996, исключительное право на которое принадлежит компаний Sugen LLC и PHARMACIA & UPJOHN COMPANY LLC.
В соответствии с пунктом 2 статьи 1362 ГК РФ если патентообладатель не может использовать изобретение, на которое он имеет исключительное право, не нарушая при этом прав обладателя другого патента (первого патента) на изобретение или полезную модель, отказавшегося от заключения лицензионного договора на условиях, соответствующих установившейся практике, обладатель патента (второго патента) имеет право обратиться в суд с иском к обладателю первого патента о предоставлении принудительной простой (неисключительной) лицензии на использование на территории Российской Федерации изобретения или полезной модели обладателя первого патента. В исковом требовании должны быть указаны предлагаемые обладателем второго патента условия предоставления ему такой лицензии, в том числе объем использования изобретения или полезной модели, размер, порядок и сроки платежей. Если этот патентообладатель, имеющий исключительное право на такое зависимое изобретение, докажет, что оно представляет собой важное техническое достижение и имеет существенные экономические преимущества перед изобретением или полезной моделью обладателя первого патента, суд принимает решение о предоставлении ему принудительной простой (неисключительной) лицензии. Полученное по этой лицензии право использования изобретения, охраняемое первым патентом, не может быть передано другим лицам, кроме случая отчуждения второго патента.
Суммарный размер платежей за принудительную простую (неисключительную) лицензию должен быть установлен в решении суда не ниже цены лицензии, определяемой при сравнимых обстоятельствах.
В случае предоставления в соответствии с этим пунктом принудительной простой (неисключительной) лицензии обладатель патента на изобретение или полезную модель, право на использование которых предоставлено на основании указанной лицензии, также имеет право на получение простой (неисключительной) лицензии на использование зависимого изобретения, в связи с которым была выдана принудительная простая (неисключительная) лицензия, на условиях, соответствующих установившейся практике.
Пунктом 3 статьи 1362 ГК РФ установлено, что на основании решения суда, предусмотренного пунктами 1 и 2 этой статьи, федеральный орган исполнительной власти по интеллектуальной собственности осуществляет государственную регистрацию предоставления и прекращения права использования изобретения на условиях принудительной простой (неисключительной) лицензии.
Как установлено судами первой и апелляционной инстанции и не оспаривается в суде кассационной инстанции ответчиками по встречному иску, обществом в адрес компаний Sugen LLC и PHARMACIA & UPJOHN COMPANY LLC направлялось предложение о заключении лицензионного договора, которое было отвергнуто последними.
Разногласия между сторонами сводятся к различной оценке обстоятельств, подлежащих установлению в целях применения пункта 2 статьи 1362 ГК РФ, а именно, в отношении использования обществом в производимом им продукте изобретения по патенту Российской Федерации N 2567535, признания зависимого изобретения важным техническим достижением и наличии у него существенных экономических преимуществ перед изобретением компаний Sugen LLC и PHARMACIA & UPJOHN COMPANY LLC.
Эксперты Лалаев Б.Ю. и Мус Г.П., исследовав регистрационное удостоверение на лекарственный препарат "Сунитиниб-натив", инструкцию по медицинскому применению этого лекарственного препарата, опытно-промышленный регламент на производство активной фармацевтической субстанции "Сунитиниба малат", патент Российской Федерации N 2567535, пришли к выводу о том, что в производимом обществом лекарственном препарате используются все признаки независимых пунктов 1 и 4 формулы изобретения по патенту Российской Федерации N 2567535.
Эксперт Мошковский С.А., исследовав те же документы, за исключением опытно-промышленного регламента, пришел к выводу о том, что изобретение по патенту Российской Федерации N 2567535 не используется в производимом обществом лекарственном препарате.
Суд первой инстанции по ходатайству сторон вызвал в судебное заседание вышеназванных экспертов для дачи ими пояснений. Указанные эксперты явились в судебное заседание, дали пояснения относительно проведенного исследования, ответили на вопросы суда и представителей сторон, в том числе сформулированные письменно.
Доводы компаний Sugen LLC и PHARMACIA & UPJOHN COMPANY LLC относительно того, что обстоятельства, связанные с использованием изобретения в лекарственном препарате, могут быть установлены исключительно путем исследования образцов этих препаратов, не может быть признан в достаточной степени обоснованным, поскольку необходимые сведения могут содержаться и в документах, характеризующих лекарственный препарат, описывающих технологические процессы по его производству. Так, эксперты Лалаев Б.Ю. и Мус Г.П. посчитали достаточными представленные для исследования источники информации для вывода об использовании произведения. Эксперт Мошковский С.А., исследовав только часть документов, вместе с тем сделал вывод о неиспользовании изобретения общества в производимом им лекарственном препарате.
Ссылаясь на невозможность использования для исследования инструкции по медицинскому применению лекарственного препарата общества и опытно-промышленного регламента, в том числе по мотиву того, что они исходят от общества, ответчики по встречному иску вместе с тем не заявили об их недостоверности, фальсификации со стороны общества.
Судом первой инстанции верно установлено, что обязательность наличия промышленного регламента, на основании которого осуществляется производство лекарственных средств, предусмотрена Законом об обращении лекарственных средств, Правилами производства и контроля качества лекарственных средств, утвержденными приказом Гостехрегулирования от 20.05.2009 N 159-ст, Отраслевым стандартом ОСТ 42-510-98 "Правила организации производства и контроля качества лекарственных средств, утвержденным Минздравом России 25.02.1998, Правилами надлежащей производственной практики, утвержденными приказом Министерства промышленности и торговли Российской Федерации от 13.06.2013 N 916.
При этом суд кассационной инстанции считает обоснованными возникшие у суда первой инстанции сомнения относительно отчета научной лаборатории (исследование неизвестного препарата, неизвестные условия хранения, транспортировки, проведение исследования на неизвестном оборудовании, с использованием неустановленных методов исследования, предельно короткий срок доставки препарата в США, исследование в лаборатории, относящейся к группе Пфайзер).
Указывая на неисследование экспертами Лалаевым Б.Ю. и Мус Г.П. отчета научной лаборатории, истцы по первоначальному иску не ссылаются на то, что указанное доказательство относилось к числу согласованных сторонами материалов исследования (пункт 4 определения о назначении судебной экспертизы от 01.06.2018).
Заключение специалиста Корлюкова А.А. также оценено судом первой инстанции как не обладающее достаточной степенью достоверности.
Ссылка компаний Sugen LLC и PHARMACIA & UPJOHN COMPANY LLC на норму части 5 статьи 69 Арбитражного процессуального кодекса Российской Федерации применительно к заключению специалиста Корлюкова А.А. не принимается судом кассационной инстанции, так как выводы, содержащиеся в заключении специалиста, не относятся к обстоятельствам, подтвержденным нотариусом при совершении нотариального действия. К таким обстоятельствам может лишь относиться факт приобретения лекарственного препарата в розничной торговле и передачи его для исследования.
Вопреки соответствующему доводу компаний Sugen LLC и PHARMACIA & UPJOHN COMPANY LLC, суды первой и апелляционной инстанций не придавали заранее установленной силы заключениям судебных экспертов Лалаева Б.Ю. и Мус Г.П., а исходили из оценки совокупности имеющихся в материалах дела доказательств, исследовав, помимо указанных заключений, также и иные доказательства, представленные сторонами. Исходя из доводов, содержащихся в кассационной жалобе истцов по первоначальному иску, очевидно, что они основаны на несогласии с той оценкой имеющихся в деле доказательств, которая была дана в обжалуемых судебных актах.
Приведенный в пункте 2 статьи 1362 ГК РФ критерий "важности технического достижения" действительно не имеет легального определения в законодательстве и в отношении его толкования не имеется устойчивой судебной практики.
Вместе с тем суд кассационной инстанции не может согласиться с доводом компаний Sugen LLC и PHARMACIA & UPJOHN COMPANY LLC о том, что суды первой и апелляционной инстанций, делая вывод о наличии этого критерия в рассматриваемом случае, исходили лишь из того, что выдача патента на изобретение общества сама по себе является доказательством важности технического достижения.
Как усматривается из обжалуемых судебных актов, суды приняли во внимание и иные обстоятельства, свидетельствующие о наличии технических преимуществ по сравнению с изобретением истцов по первоначальному иску, в том числе пришли к выводу о том, что разница в скорости появления действующего вещества в крови кроликов и то, что сунитиниб может демонстрировать полиформизм, подтверждают важность технического достижения изобретения по патенту общества. Указанные два явления подробно исследованы в заключениях экспертов Лалаева Б.Ю. и Мус Г.П., которые с использованием научных источников и, опираясь на пример эксперимента в описании к патенту, пришли к выводу о том, что зависимое изобретение истца следует рассматривать как важное техническое достижение.
При таких обстоятельствах у судов первой и апелляционной инстанций имелись достаточные основания для того, чтобы согласиться с мнением названных судебных экспертов.
Заявляя о непроведении обществом полноценных клинических исследований, подтверждающих терапевтические преимущества зависимого изобретения, истцы по первоначальному иску вместе с тем не представили доказательств, опровергающих результаты эксперимента и полиморфизм сунитиниба.
С учетом изложенного коллегия судей не находит оснований для переоценки выводов судов первой и апелляционной инстанций в части признания зависимого изобретения общества важным техническим достижением, которые сделаны на основании оценки доводов сторон и представленных в материалы дела доказательств.
Не усматривает Суд по интеллектуальным правам и достаточных оснований для признания необоснованными выводов судов первой и апелляционной инстанции, касающихся экономических преимуществ изобретения общества перед изобретением по патенту истцов по первоначальному иску.
Применительно к указанному условию для предоставления принудительной лицензии в российском законодательстве также отсутствует определение понятия "существенные экономические преимущества одного изобретения по отношению к другому" и выработанные судебной практикой подходы.
Суд первой инстанции, признавая, что изобретение общества имеет существенные экономические преимущества по отношению к изобретению компаний Sugen LLC и PHARMACIA & UPJOHN COMPANY LLC, принял во внимание заключение эксперта Лалаева Б.Ю. и заключение заведующего сектором гражданского права Института государства и права Российской академии наук Санниковой Л.В., согласился с изложенным в них и расчете общества мнением о том, что поскольку первоначальная предельная отпускная цена на препарат истца по встречному иску меньше как минимум на 20% относительно цены препарата истцов по первоначальному иску, а при проведении торгов разница в цене препаратов может достигнуть 60% и с учетом годового объема только государственных закупок согласно расчету истца по встречному иску годовая экономия бюджетных средств только по одному спорному препарату превысит 200 000 000 рублей.
При этом компании Sugen LLC и PHARMACIA & UPJOHN COMPANY LLC, подвергая критике расчет общества, и ссылаясь на наличие у них значительных затрат, какие-либо обоснованные расчеты не представили, указав лишь на инвестирование в разработку лекарственного препарата "Сутент" около 1 млрд. долларов США и не представив доказательств этого утверждения.
Приложенные к кассационной жалобе заключения специалистов Ворожевич А.С., Третьякова С.В., Старженецкого В.В., Костина А.В. и Ягудиной Р.И., относящиеся к вопросам толкования понятий "важное техническое достижение" и "существенные экономические преимущества", а также приложенное к дополнению к кассационной жалобе письмо Роспатента от 10.07.2019 N 02/24-11482, которые не представлялись при рассмотрении дела судами первой и апелляционной инстанций, не могут быть учтены судом кассационной инстанции в силу отсутствия у него полномочий по установлению обстоятельств, принятию и оценке новых доказательств, в связи с чем были возвращены компаниям Sugen LLC и PHARMACIA & UPJOHN COMPANY LLC в судебном заседании.
При этом коллегия судей отмечает, что в силу части 1 статьи 65 Арбитражного процессуального кодекса Российской Федерации каждое лицо, участвующее в деле, должно доказать обстоятельства, на которые оно ссылается как на основание своих требований и возражений, а согласно части 2 статьи 9 этого Кодекса лица, участвующие в деле, несут риск наступления последствий совершения или несовершения ими процессуальных действий.
Отсутствие в патенте общества сведений, которые могли бы свидетельствовать о наличии экономической эффективности основанного на этом изобретении препарата, не является обстоятельством, которое опровергает выводы судов о наличии у зависимого изобретения существенных экономических преимуществ, так как экономическая эффективность не отнесена к заявленным техническим результатам изобретения общества.
Ссылка истцов по первоначальному иску на отсутствие у эксперта Лалаева Б.Ю. и заведующего сектором гражданского права Института государства и права Российской академии наук Санниковой Л.В. необходимой квалификации для исследования вопроса о существенных экономических преимуществах зависимого изобретения не принимается судом кассационной инстанции, поскольку истцами по первоначальному иску при рассмотрении судом первой инстанции вопроса о назначении судебной экспертизы не предлагались кандидатуры экспертов, обладающих экономическим образованием, а вывод являющегося по специальности биологом эксперта Мошковского С.А. об отсутствии экономических преимуществ зависимого изобретения не вызывает у указанных лиц сомнений. При обращении с ходатайством о назначении повторной судебной экспертизы истцы по первоначальному иску также не предлагали в качестве экспертов для исследования вопроса о наличии существенных экономических преимуществах специалистов, обладающих экономическим образованием.
Ссылаясь на то, что установление стоимости лицензии в размере 10% от доходной части цены на лекарственный препарат общества не соответствует общепринятым условиям лицензирования при сравнимых обстоятельствах и данные платежи не смогут обеспечить получение хоть какой-то прибыли истцами по первоначальному иску, компании Sugen LLC и PHARMACIA & UPJOHN COMPANY LLC вместе с тем не представили доказательств данных утверждений и соответствующих расчетов.
Судом кассационной инстанции не могут быть признаны обоснованными доводы истцов по первоначальному иску о пристрастности экспертов Лалаева Б.Ю. и Мус Г.П., а также о наличии оснований для отвода этих экспертов. Судом первой инстанции верно установлено, что указанные доводы связаны с несогласием истцов по первоначальному иску с выводами указанных экспертов. При этом истцами по первоначальному иску не представлены какие-либо доказательства заинтересованности данных экспертов в исходе дела.
Ссылка компании Sugen LLC в дополнении к кассационной жалобе на то, что заключение эксперта Мус Г.П. аналогично заключению эксперта Семенова В.И., составленному в рамках дела N А40-71471/2017, не принимается судом кассационной инстанции, так как этот довод не заявлялся при рассмотрении дела в судах первой и апелляционной инстанций, а заключение эксперта Семенова В.И. представлено только в суд кассационной инстанции, в связи с чем было возвращено лицу, подавшему дополнение к кассационной жалобе.
Судом по интеллектуальным правам также отклоняется довод компаний Sugen LLC и PHARMACIA & UPJOHN COMPANY LLC о том, что суды первой и апелляционной инстанций необоснованно отказали в удовлетворении их ходатайств о назначении повторной судебной экспертизы.
Повторная экспертиза в силу части 2 статьи 87 Арбитражного процессуального кодекса Российской Федерации в случае возникновения сомнений в обоснованности заключения эксперта или наличия противоречий в выводах эксперта или комиссии экспертов.
Между тем, отказывая в удовлетворении ходатайств о назначении повторной судебной экспертизы, суды первой и апелляционной инстанций обоснованно исходили из отсутствия сомнений в обоснованности заключений и отсутствия противоречий, поскольку все имеющиеся вопросы были разрешены в ходе опроса экспертов в судебном заседании суда первой инстанции, заявителями данных ходатайств не представлено достаточных доказательств, подтверждающих необходимость повторного исследования вопросов, стоявших перед экспертами.
Ссылка компании Sugen LLC на то, что в рассматриваемом случае суды должны были назначить дополнительную судебную экспертизу не принимается Судом по интеллектуальным правам, поскольку такое ходатайство истцами по первоначальному иску не заявлялось ни в суде первой, ни в суде апелляционной инстанции.
Довод компаний Sugen LLC и PHARMACIA & UPJOHN COMPANY LLC о том, что встречный иск не мог быть принят к рассмотрению в силу того, что истец по встречному иску на момент обращения с этим иском не являлся правообладателем патента Российской Федерации N 2567535, подлежит отклонению по следующим основаниям.
Как усматривается из материалов дела, договор об отчуждении исключительного права на изобретение по патенту Российской Федерации N 2567535 N 1С был заключен между Михайловым О.Р. (прежним правообладателем патента) и обществом 09.02.2018, а встречное исковое заявление подано в Арбитражный суд города Москвы 27.02.2018, государственная регистрация указанного договора произведена Роспатентом 23.03.2018.
Таким образом, на момент обращения со встречным иском общество являлось правопреемником в отношении патента Российской Федерации N 2567535, в связи с чем у суда первой инстанции первой инстанции не имелось оснований для непринятия встречного искового заявления к производству. При этом истцы по первоначальному иску при рассмотрении судом первой инстанции вопроса о принятии встречного иска к производству не ссылались на то, что общество на момент обращения со встречным иском не являлось правообладателем патента Российской Федерации N 2567535, приводя в качестве возражений ссылки на иные обстоятельства.
Судом кассационной инстанции не принимается довод истцов по первоначальному иску о том, что в нарушение пункта 2 статьи 1362 ГК РФ суды обязали истцов выдать обществу принудительную лицензию на использование сунитиниба во всех его формах, а не только на кристаллическую модификацию, охраняемую патентом общества, так как такой вывод не следует из резолютивной части обжалуемого решения, поскольку в резолютивной части имеется указание на лекарственный препарат "Сунитиниб-натив", который основан на патенте общества, устанавливающем правовую охрану кристаллической модификации сунитиниба. При этом из мотивировочной части четко следует, что принудительная лицензия выдается только в целях использования зависимого изобретения.
Ссылка компаний Sugen LLC и PHARMACIA & UPJOHN COMPANY LLC на то, что резолютивная часть решения суда первой инстанции не соответствует в части заявленным обществом требованиям по встречному иску не принимается судом кассационной инстанции как обстоятельство, влекущее за собой отмену судебных актов, поскольку соответствующий довод не заявлялся указанными лицами в суде апелляционной инстанции, не был предметом исследования со стороны апелляционного суда. При этом данное "несоответствие" не свидетельствует о выходе суда первой инстанции за пределы заявленных требований, так как представляет собой уточнение формулы расчета стоимости лицензии применительно к лекарственному препарату "Сунитиниб-натив".
Не имеется у коллегии судей кассационной инстанции и оснований для вывода о том, что обжалуемые судебные акты приняты об обязанностях Роспатента, поскольку ни мотивировочная, ни резолютивная части решения не содержат указания на обязанность Роспатента зарегистрировать договор принудительной простой (неисключительной) лицензии, а возлагают такую обязанность на ответчиков по встречному иску. При этом судом кассационной инстанции также учитывается, что Роспатент не обращался в суд с жалобой в порядке, предусмотренном статьей 42 Арбитражного процессуального кодекса Российской Федерации.
Кроме того, согласно разъяснению, данному в пункте 53 совместного постановления Пленума Верховного Суда Российской Федерации и Пленума Высшего Арбитражного Суда Российской Федерации от 29.04.2010 N 10/22 "О некоторых вопросах, возникающих в судебной практике при разрешении споров, связанных с защитой права собственности и других вещных прав", в силу части 1 статьи 16 Арбитражного процессуального кодекса Российской Федерации обязанность совершения действий по государственной регистрации возложена на уполномоченный государственный орган независимо от его участия в деле. Указанное разъяснение, сформулированное применительно к регистрации вещных прав, вместе с тем применимо и к отношениям, связанным с интеллектуальной собственностью.
С учетом изложенного у суда кассационной инстанции отсутствуют достаточные основания для отмены обжалуемых судебных актов на основании доводов, изложенных в кассационной жалобе компаний Sugen LLC и PHARMACIA & UPJOHN COMPANY LLC.
Вместе с тем Судом по интеллектуальным правам не усматривается и оснований для удовлетворения кассационной жалобы общества, в которой содержится требование об изменении обжалуемых судебных актов в части возложения на ответчиков по встречному иску обязанности зарегистрировать договор принудительной простой (неисключительной) лицензии.
Как правильно указано судом апелляционной инстанции в обжалуемом постановлении, исковое требование обязать ответчиков по встречному иску "совершить необходимые действия для осуществления государственной регистрации договора" во встречном исковом заявлении отсутствовало, в связи с чем суд первой инстанции рассматривал встречные исковые требования в том виде, в каком они были заявлены. Суд кассационной инстанции соглашается с указанной оценкой доводов общества.
С учетом изложенного, рассмотрев кассационные жалобы в пределах изложенных в ней доводов, коллегия судей полагает, что фактические обстоятельства, имеющие значение для дела, установлены судами первой и апелляционной инстанций на основании объективного исследования имеющихся в деле доказательств с учетом доводов и возражений участвующих в деле лиц, выводы судов соответствуют фактическим обстоятельствам и представленным доказательствам, в целом основаны на правильном применении норм материального и процессуального права.
Судом кассационной инстанции также принимается во внимание разъяснение, содержащееся в постановлении Президиума Высшего Арбитражного Суда Российской Федерации от 23.04.2013 N 16549/12, согласно которому из принципа правовой определенности следует, что решение суда первой инстанции, основанное на полном и всестороннем исследовании обстоятельств дела, не может быть отменено исключительно по мотиву несогласия с оценкой указанных обстоятельств, данной судом первой инстанции.
В соответствии с правовой позицией Конституционного Суда Российской Федерации, приведенной, в том числе в определении от 17.02.2015 N 274-О, статьи 286-288 Арбитражного процессуального кодекса Российской Федерации, находясь в системной связи с другими положениями данного Кодекса, регламентирующими производство в суде кассационной инстанции, предоставляют суду кассационной инстанции при проверке судебных актов право оценивать лишь правильность применения нижестоящими судами норм материального и процессуального права и не позволяют ему непосредственно исследовать доказательства и устанавливать фактические обстоятельства дела.
Иное позволяло бы суду кассационной инстанции подменять суды первой и второй инстанций, которые самостоятельно исследуют и оценивают доказательства, устанавливают фактические обстоятельства дела на основе принципов состязательности, равноправия сторон и непосредственности судебного разбирательства, что недопустимо.
Из изложенного следует, что суд кассационной инстанции не вправе устанавливать или считать доказанными обстоятельства, которые не были установлены в решении или постановлении нижестоящих судов либо были отвергнуты судами первой или апелляционной инстанций, предрешать вопросы о достоверности или недостоверности того или иного доказательства, преимуществе одних доказательств перед другими; не наделен полномочиями по исследованию и оценке доказательств, установлению фактических обстоятельств дела, которые не были установлены судами первой и апелляционной инстанций, приобщению к материалам дела дополнительных доказательств, которые не были предметом оценки в судах, рассматривающих спор по существа, их оценке и другими, что означает отсутствие у суда кассационной инстанции необходимых процессуальных механизмов, присущих суду первой инстанции при рассмотрении дела.
Нарушений норм процессуального права, которые в силу части 4 статьи 288 Арбитражного процессуального кодекса Российской Федерации могут являться основанием для отмены судебных актов судов первой и апелляционной инстанций в любом случае, судом кассационной инстанции не установлено.
Таким образом, обжалуемые судебные акты являются законными и отмене не подлежат. Оснований для удовлетворения кассационных жалоб не имеется.
Расходы по уплате государственной пошлины за подачу кассационной жалобы в соответствии с частью 1 статьи 110 Арбитражного процессуального кодекса Российской Федерации относятся на заявителей этих жалоб.
Руководствуясь статьями 286, 287, 288, 289 Арбитражного процессуального кодекса Российской Федерации, суд
ПОСТАНОВИЛ:
решение Арбитражного суда города Москвы от 08.02.2019 по делу N А40-166505/2017 и постановление Девятого апелляционного арбитражного суда от 07.05.2019 по тому же делу оставить без изменения, кассационные жалобы общества с ограниченной ответственностью "Натива", иностранных лиц - Sugen LLC и PHARMACIA & UPJOHN COMPANY LLC - без удовлетворения.
Постановление вступает в законную силу со дня его принятия и может быть обжаловано в кассационном порядке в Судебную коллегию Верховного Суда Российской Федерации в двухмесячный срок.
| Председательствующий судья | А.А. Снегур |
| Судья | Р.В. Силаев |
| Судья | Е.С. Четвертакова |
Обзор документа
Иностранные фармкомпании потребовали от российского производителя прекратить нарушение евразийского патента на противоопухолевый американский препарат. Российская компания, в свою очередь, требовала от них принудительную лицензию на выпуск аналога с применением собственных разработок. Она выиграла спор во всех инстанциях, в том числе в Суде по интеллектуальным правам.
Принудительная лицензия предоставляется при использовании зависимого изобретения для создания новых улучшенных версий запатентованных препаратов. Эксперты признали спорное изобретение зависимым от охраняемого, а препарат - важным техническим достижением, так как он всасывается в кровь быстрее оригинала и имеет экономические преимущества, поскольку дешевле. Кроме того, российский дженерик социально значим, включен в список ЖНВЛП.



(1).jpg)


