Методические рекомендации МР 4.2.0249-21 “Серологическая диагностика острых кишечных инфекций методом РПГА (шигеллеза, сальмонеллеза и брюшного тифа)” (утв. Федеральной службой по надзору в сфере защиты прав потребителей и благополучия человека, Главным государственным санитарным врачом РФ 20 мая 2021 г.) (документ не вступил в силу)
Методические рекомендации МР 4.2.0249-21
“Серологическая диагностика острых кишечных инфекций методом РПГА (шигеллеза, сальмонеллеза и брюшного тифа)”
(утв. Федеральной службой по надзору в сфере защиты прав потребителей и благополучия человека, Главным государственным санитарным врачом РФ 20 мая 2021 г.)
Дата введения: 1 сентября 2021 г.
I. Область применения
1.1. В настоящих методических рекомендациях (далее - МР) представлены методы применения реакции пассивной гемагглютинации (далее - РПГА) при серологической диагностике шигеллеза и сальмонеллеза, включая брюшной тиф и паратифы, и выявлении хронических бактерионосителей возбудителя брюшного тифа, а также методика определения иммуноглобулинов класса G (далее - IgG) с использованием редуцирующих веществ.
1.2. МР разработаны с целью унифицирования использования РПГА при шигеллезе, вызванном Shigella sonnei и Shigella flexneri, сальмонеллезе, вызванной Salmonella серологических групп О2(A), О4(B), О7( ), О8(
), О8(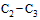 ), О9(
), О9(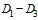 ), О3,10(E), и интерпретации результатов с учетом клинической выраженности заболевания и активности эпидемического процесса на конкретной территории.
), О3,10(E), и интерпретации результатов с учетом клинической выраженности заболевания и активности эпидемического процесса на конкретной территории.
1.3. МР предназначены для органов и организаций Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека, а также могут быть использованы научными и медицинскими организациями, осуществляющими серологическую диагностику острых кишечных инфекций (далее - ОКИ).
II. Общие положения
2.1. Диагнозы шигеллез и сальмонеллез, включая брюшной тиф и паратифы, определяются на основании клинических признаков заболевания с учетом эпидемиологического анамнеза и результатов комплексного лабораторного обследования с использованием бактериологического (культурального), молекулярно-генетического и серологического методов, соответствующих санитарно-эпидемиологическим требованиям1 и методическим документам2. Бактериологическая диагностика имеет приоритетное значение, так как выделение возбудителя позволяет получить полную информацию о его фенотипических свойствах, включая чувствительность к антибиотикам.
2.2. Серологический метод диагностики шигеллеза, сальмонеллеза, брюшного тифа и паратифов является ретроспективным, регистрирует иммунный ответ макроорганизма на инфицирование возбудителем - появление специфических антител к О-антигенам Shigella и Salmonella и Vi-антигену возбудителя брюшного тифа и паратифа С. Диагностическое значение имеет определение в сыворотке крови инфицированных лиц количественного содержания (уровня) суммарных антител и IgG.
2.3. Серологическая диагностика способствует совершенствованию системы эпидемиологического надзора за ОКИ, так как количественная и качественная характеристика иммунного ответа на встречу с возбудителями позволяет диагностировать стертые и субклинические формы болезни, выявлять ранее переболевших, обеспечивает более полную и обоснованную информацию для оценки активности эпидемического процесса.
2.4. Серологический метод позволяет дифференцировать транзиторное носи- тельство от субклинической формы брюшного тифа. При транзиторном носительстве отсутствует достоверный сдвиг в уровнях сывороточных антител. Наличие положительной динамики указывает на развитие патологического процесса, который может характеризоваться субклиническим течением.
В настоящее время более 60% ОКИ остаются бактериологически нерасшифрованными. Выявление антител и определение их класса может использоваться для оперативного эпидемиологического анализа в очагах ОКИ с целью уточнения фактической распространенности инфекции в коллективе и поиска источника. Быстрое и полное выявление всех инфицированных в очаге позволяет конкретизировать профилактические, противоэпидемические, лечебные мероприятия и способствует ликвидации очага.
III. Материально-техническое обеспечение метода3
3.1. Для проведения РПГА используют стандартное общелабораторное оборудование и материалы:
- термостат, позволяющий поддерживать рабочую температуру плюс 37°С плюс/минус 1°С;
- водяная баня или термостат, поддерживающие температуру плюс 56°С плюс/минус 1°С;
- холодильник, поддерживающий температуру от плюс 2 до плюс 8°С;
- морозильная камера, поддерживающая температуру не выше минус 16°С;
- центрифуга лабораторная, 2,5 - 3,0 тыс. оборотов в минуту;
- одноканальные дозаторы переменного объема с диапазоном объема доз от 20 до 1000 мкл;
- многоканальные дозаторы переменного объема, объем дозы 50 мкл;
- дозатор одноканальный для пошагового дозирования (по типу степпер), объем дозы 25 мкл;
- автоматический встряхиватель (шейкер) для пробирок;
- система для взятия крови по типу «Вакутейнер» (англ. Vacutainer) без наполнителя или с активатором свертывания;
- микропробирки на 1,5-2,0 мл (по типу «Эппендорф»);
- стерильные пробирки (многоразового или однократного использования), объем 10 мл;
- планшеты круглодонные для иммунологических реакций однократного применения;
- одноразовые наконечники для дозаторов переменного объема от 20 мкл до 1000 мкл;
- емкость с дезинфицирующим раствором4.
3.2. Наборы диагностикумов и реагенты, зарегистрированные и разрешенные для использования на территории Российской Федерации в установленном порядке5:
- эритроцитарные диагностикумы для постановки РПГА;
- редуценты: L-цистеин; унитиол 50 мг/мл (димеркаптоопропансульфонат натрия);
- стерильный физиологический раствор (0,9% раствор натрия хлорида), pH 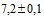 (может входить в набор диагностикумов).
(может входить в набор диагностикумов).
3.3. Для серодиагностики бактериальных ОКИ могут применяться следующие эритроцитарные диагностикумы, зарегистрированные в государственном реестре медицинских изделий и организаций (индивидуальных предпринимателей)6:
- диагностикум эритроцитарный сальмонеллезный комплексный серогрупп А, В,  ,
, 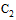 , D, Е (антигены 1; 2; 3; 4; 6; 7; 8; 9; 10; 12), жидкий;
, D, Е (антигены 1; 2; 3; 4; 6; 7; 8; 9; 10; 12), жидкий;
- диагностикумы эритроцитарные сальмонеллезные О-антигенные групповые - серогрупп А (антигены 1, 2, 12); В (антигены 1, 4, 12); C1 (антигены 6, 7); 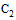 (антигены 6, 8); D (антигены 1, 9,12); Е (антигены 3,10), жидкие;
(антигены 6, 8); D (антигены 1, 9,12); Е (антигены 3,10), жидкие;
- диагностикум эритроцитарный сальмонеллезный Ви-антигенный, жидкий;
- диагностикум эритроцитарный сальмонеллезный Vi-антигенный, сухой;
- диагностикумы эритроцитарные шигеллезные: Зонне антигенный, жидкий; Зонне антигенный, сухой; Флекснера 1-5 антигенный, жидкий; Флекснера 1-5 антигенный, сухой; Флекснера 6 антигенный, сухой.
IV. Диагностикумы эритроцитарные
4.1. Диагностикумы эритроцитарные для постановки РПГА содержат специфические О-антигены бактерий рода Shigella и Salmonella, а также Vi-антиген возбудителя брюшного тифа и паратифа С, фиксированные на поверхности эритроцитов. При взаимодействии сенсибилизированных эритроцитов с гомологичными антителами в сыворотке крови инфицированных лиц наблюдается феномен агглютинации эритроцитов.
4.2. Жидкие диагностикумы представляют собой 1%-ю или 0,75%-ю взвесь формалинизированных эритроцитов, сенсибилизированных соответствующими антигенами Shigella и Salmonella, в фосфатном буферном растворе. Препараты представляют собой гомогенную непрозрачную суспензию коричневого цвета (окраска взвешенных в жидкости формалинизированных эритроцитов). При хранении диагностикумов эритроциты оседают, образуя плотный коричневый осадок и прозрачную желтоватую надосадочную жидкость.
4.3. Сухие диагностикумы представляют собой 5%-ю или 10%-ю взвесь форма- линизированных и сенсибилизированных соответствующими О-антигенами Shigella и Salmonella эритроцитов, высушенных в сахарозо-желатиновой среде или боратно-янтарном буферном растворе с добавлением мясопептонного бульона и сахарозы.
V. Получение сыворотки крови
5.1. Для серологических исследований используют сыворотку крови (прозрачная, негемолизированная, без видимых глазом эритроцитов). Объем сыворотки зависит от количества используемых диагностикумов, а также необходимости исследования парных сывороток и определения класса антител.
5.2. Кровь собирают согласно методическим указаниям7 с соблюдением правил асептики в стерильную пробирку с использованием системы по типу «Вакутейнер» (англ. Vacutainer) без наполнителя или с активатором свертывания или аналогичной, разрешенной к применению в Российской Федерации.
5.3. Не позднее 24 часов после взятия крови сыворотку отделяют и переносят в стерильную пробирку. Для этого пробирки с кровью оставляют до образования сгустка при комнатной температуре на 1-2 часа или помещают в термостат при плюс 37°С на 10-15 минут. При необходимости образовавшийся сгусток отслаивают от стенок пробирки (например, бактериологической петлей). Для лучшей ретракции сгустка и более полного отделения сыворотки пробу выдерживают при плюс 4°С в холодильнике в течение 1 часа или центрифугируют 5-10 минут при 2,5-3,0 тыс. об/мин.
Если сыворотка содержит примесь эритроцитов, ее центрифугируют при условиях, указанных в первом абзаце п. 5.3.
5.4. Для уменьшения «неспецифической» агглютинации, которая может наблюдаться у части обследуемых лиц (особенно у лихорадящих больных) из-за присутствия пирогенов, C-реактивного белка и других термолабильных факторов, перед постановкой РПГА сыворотку инактивируют - прогревают при плюс 56°С в течение 30 минут.
5.5. Инактивированные сыворотки хранят в условиях, предотвращающих бактериальный пророст, при температуре от плюс 2°С до плюс 8°С не более 72 часов. Допускается хранение в течение 6 мес. при минус 16 - минус 20°С в микропробирках на 1,5-2,0 мл (по типу «Эппендорф») при условии однократного размораживания.
VI. Постановка РПГА микрометодом
6.1. РПГА проводят микрометодом в планшетах (круглодонных для иммунологических реакций однократного применения) с использованием автоматических дозаторов. Объем титруемой сыворотки составляет 0,05 мл (50 мкл). При исследовании нескольких диагностикумов использование многоканальных дозаторов ускоряет исследование, поскольку позволяет проводить разведение сыворотки синхронно в нескольких рядах планшета.
6.2. В случае если физиологический раствор (0,9%-й раствор натрия хлорида, pH  ) не входит в набор с диагностикумами (п. 3.2), то допускается его приготовление из химически чистого хлористого натрия (NaCl) на дважды дистиллированной или деионизированной воде (с целью предотвращения незначительных количеств солей металлов, которые могут вызвать гемолиз эритроцитов или их агглютинацию).
) не входит в набор с диагностикумами (п. 3.2), то допускается его приготовление из химически чистого хлористого натрия (NaCl) на дважды дистиллированной или деионизированной воде (с целью предотвращения незначительных количеств солей металлов, которые могут вызвать гемолиз эритроцитов или их агглютинацию).
6.3. Исследование сыворотки:
- у взрослых и детей старше 12 лет начинают с разведения 1:50 (последнее разведение 1:1600);
- у детей от 6 до 12 лет - с разведения 1:25 (последнее разведение 1:400);
- у детей младше 6 лет применять диагностику ОКИ серологическим методом - нецелесообразно (см. главу XIII);
- для выявления антител к Vi-антигену - с разведения 1:10 вне зависимости от возраста обследуемого (последнее разведение 1:320).
6.4. Учитывая последующее двукратное разбавление сыворотки в лунках планшета 0,9%-м раствором натрия хлорида, необходимо приготовить в отдельной пробирке рабочее разведение сыворотки: для взрослых - 1:25 (например, 0,1 мл сыворотки + 2,4 мл 0,9%-го раствора натрия хлорида); для детей - 1:5 (например, 0,1 мл сыворотки + 0,4 мл 0,9%-го раствора натрия хлорида). Объем сыворотки зависит от количества используемых диагностикумов: для каждого диагностикума необходимо 0,05 мл рабочего разведения сыворотки, для постановки контроля - дополнительно 0,2 мл. Например, при исследовании сыворотки с четырьмя диагностикумами необходимо приготовить не менее 0,5 мл рабочего разведения: (0,05 х 4) + 0,2 + 0,1 (на потери в процессе постановки).
6.5. Последовательные двукратные разведения сывороток готовят непосредственно в планшетах, используя для этого один ряд для каждого диагностикума (достаточно 5-6 лунок в ряду). Во все лунки ряда вносят по 0,05 мл 0,9%-го раствора натрия хлорида.
6.6. В первую лунку ряда вносят 0,05 мл из пробирки с рабочим разведением (п. 6.4) и получают разведение 1:50 (1:10 для детей или при выявлении антител к Vi-антигену). Затем делают серию последовательных разведений путем переноса 0,05 мл сыворотки из предыдущей лунки (начиная с первой) в следующую лунку ряда (заполненную тем же количеством 0,9%-го раствора натрия хлорида). При переносе содержимое лунки аккуратно перемешивают, избегая образования пузырьков. Из последней лунки удаляют 0,05 мл для сохранения одинакового объема сыворотки (в емкость с дезинфицирующим раствором).
6.7. Перед использованием флакон с диагностикумом осторожно встряхивают до получения гомогенной взвеси и полного исчезновения осадка на дне.
6.8. В каждую из лунок ряда с разведениями сыворотки добавляют соответствующий диагностикум в объеме согласно инструкции производителя (например, по 0,025 мл).
6.9. Планшеты после внесения диагностикума осторожно встряхивают и помещают в термостат при температуре 37 плюс/минус 1°С. Учет реакции проводят согласно инструкции производителя.
VII. Контроли специфичности РПГА
7.1. Подтверждение агглютинации диагностикума с сывороткой диагностической, содержащей гомологичные антигены (сальмонеллезные или шигеллезные), прикладываемой к диагностикуму: развести сухую диагностическую сыворотку согласно инструкции производителя, приготовить ряд последовательных двукратных разведений (начиная с 1 : 100 до титра, указанного на этикетке флакона сыворотки), в каждую лунку ряда добавить 0,025 мл диагностикума (аналогично пунктам 6.6 - 6.8),
7.2. Подтверждение отсутствия спонтанной агглютинации диагностикума: в две свободные лунки планшета добавить по 0,05 мл физиологического раствора и 0,025 мл диагностикума.
7.3. Подтверждение отсутствия в испытуемой сыворотке агглютининов к эритроцитам барана (контроль для диагностикумов на основе эритроцитов барана): в две свободные лунки планшета внести по 0,05 мл рабочего разведения исследуемой сыворотки и 0,025 мл 1%-й взвеси несенсибилизированных формалинизированных эритроцитов барана, которые прилагаются к диагностикуму (контрольные эритроциты).
7.4. Проверка отсутствия хлопьев в исследуемой сыворотке (обязательный контроль): в две свободные лунки планшета внести по 0,05 мл рабочего разведения исследуемой сыворотки.
VIII. Учет результатов РПГА
8.1. Результаты РПГА для исследуемой сыворотки учитываются в том случае, если все контроли дали удовлетворительные результаты:
- отмечена агглютинация диагностикума с гомологичной диагностической сывороткой в разведении, указанном производителем (не менее чем на «3+», п. 8.2);
- отсутствует спонтанная агглютинация диагностикума в 0,9%-м,растворе хлорида натрия: все эритроциты должны осесть на дне лунки в виде «пуговки»;
- отсутствует агглютинация несенсибилизированных эритроцитов барана с испытуемой сывороткой: все эритроциты должны осесть на дне лунки в виде «пуговки»;
- испытуемая сыворотка не содержит хлопьев и осадка.
8.2. Учет результатов РПГА проводится по четырехкрестной системе (если производитель не приводит другую систему учета результатов):
- «4+» или «++++»: все эритроциты агглютинированы и равномерно покрывают дно лунки в виде «зонтика»;
- «3+» или «+++»: агглютинированы почти все эритроциты, на их фоне имеется мало заметное кольцо из осевших неагглютинированных эритроцитов;
- «2+» или «++»: наряду с равномерным агглютинатом на дне лунки имеется осадок из неагглютинированных эритроцитов в виде «колечка» или «пуговки»;
- «1+» или «+»: большинство эритроцитов неагглютинировано и осело в центре дна лунки в виде маленького «колечка» или «пуговки»;
- «-»: признаков агглютинации нет, эритроциты осели в центре дна лунки в виде маленького «колечка» или “пуговки” с ровными краями.
8.3. Уровень антител в исследуемой пробе равен последнему разведению сыворотки, которое дает ярко выраженную агглютинацию эритроцитов не менее чем на «3+».
IX. Определение уровня антител класса IgG
9.1. Наиболее доступным способом разделения антител классов IgM и IgG является разрушение макроглобулиновых антител (к которым относятся молекулы IgM) с помощью редуцентов. Под действием редуцирующих веществ IgM-антитела расщепляются с разрывом дисульфидных связей молекул белка, диссоциируя при этом на 6-8 мономеров, не обладающих активностью антител. Антитела класса IgG устойчивы к действию редуцентов и не разрушаются. Однако этот метод не позволяет оценить наличие IgM, если их количество в сыворотке меньше или равно антителам класса IgG.
9.2. В качестве редуцирующих веществ используют L-цистеин (солянокислый, или «свободный»), цистин, меркаптоэтанол, унитиол, этантиол, и др.
9.3. Для обработки сывороток 5%-й раствор унитиола (50 мг/мл) разводят в стерильной пробирке в 4 раза 0,9%-м раствором натрия хлорида до получения концентрации 1,25%, т. е. к 1 объему 5%-го раствора унитиола добавляют 3 объема 0,9%-го раствора натрия хлорида. Приготовленный таким образом 1,25%-й раствор унитиола можно хранить в холодильнике при плюс 4°С в течение недели в пробирке с хорошо притертой воздухонепроницаемой пробкой.
Исследуемую инактивированную сыворотку разводят 1:5 в 0,9%-м растворе натрия хлорида и делят на 2 равные порции. К одной порции добавляют равный объем 1,25%-го раствора унитиола, к другой - равный объем 0,9%-го раствора натрия хлорида: Смешивание проводят в стерильных пробирках, которые плотно закрывают воздухонепроницаемыми пробками (или по типу «Эппендорф»). Обе порции сыворотки (обработанную редуцентом и необработанную) оставляют на 18 часов при комнатной температуре или на 2 часа в условиях термостата (плюс 37°С), затем исследуют в РПГА с диагностикумами по вышеописанной методике, начиная с разведения 1:10.
9.4. Методика использования L-цистеина как редуцента приведена в методических указаниях8. В виду легкой окисляемости раствор готовят непосредственно перед применением и хранят не более 1 часа. Для этого 15,0 мг солянокислого L-цистеина или «свободного» цистеина растворяют в 1,0 мл 0,1 N раствора едкого натра (pH готового раствора 7,0 - 7,2).
Исследуемую инактивированную сыворотку разводят 1:5 в 0,9%-м растворе натрия хлорида и делят на 2 равные порции. К одной порции добавляют равный объем раствора цистеина, к другой - равный объем 0,9%-го раствора натрия хлорида. Смешивание проводят в стерильных пробирках, которые плотно закрывают воздухонепроницаемыми пробками (или по типу «Эппендорф»). Для уменьшения инактивации цистеина кислородом воздуха между содержимым пробирки и пробкой должно оставаться минимальное свободное пространство. Пробирки с обработанными и необработанными сыворотками выдерживают в течение 18-20 часов в термостате при плюс 37°С. Затем обе пробы сыворотки исследуют в РПГА с диагностикумами по вышеописанной методике, начиная с разведения 1:10, при этом в раствор для титрования добавляют 1% нормальной инактивированной сыворотки крови (лошадиной, кроличьей, крупного рогатого скота), проверенной на отсутствие антител к применяемым диагностикумам.
9.5. Парные сыворотки всегда исследуются в одном опыте с одним диагностикумом: при определении суммарных антител и уточнении их класса.
X. Критерии постановки диагноза по результатам серологического исследования сыворотки крови
10.1. Диагноз шигеллеза или сальмонеллеза по результатам исследования сывороток на наличие антител к возбудителям может быть основан на:
- констатации так называемого «диагностического» уровня антител класса IgG при однократном исследовании сыворотки крови, взятой не ранее 7-8-го дня болезни;
- выявлении достоверного изменения уровня антител класса IgG при одновременном исследовании парных проб сывороток, взятых в динамике заболевания с интервалом 7-8 дней.
На поздних сроках заболевания уровень антител в первой сыворотке может превышать диагностический уровень и не иметь достоверного увеличения во второй сыворотке.
XI. Интерпретация результатов РПГА с использованием критерия «диагностический уровень»
11.1. Условно-диагностический уровень антител при исследовании нативной сыворотки (взятой не ранее 7-8-го дня заболевания) от больных с клиническими симптомами шигеллеза или сальмонеллеза, при исследовании с диагностикумами шигел- лезными (Зонне и Флекснера), сальмонеллезными (комплексным или серогрупп А, В, С1, С2, D и Е) составляет:
- для суммарных антител: 1:100 для взрослых и детей старше 6 лет;
- для антител класса IgG: 1:20 - 1:40.
11.2. Условно-диагностический уровень антител при исследовании нативной сыворотки (взятой не ранее 7-го дня заболевания, после окончания лихорадочного периода) от взрослых больных и детей старше 6 лет с подозрением на брюшной тиф и пара-тифы при исследовании с диагностикумами сальмонеллезными серогрупп А, В, 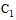 и D, составляет для суммарных антител 1:100, для IgG 1:20 - 1:40. Значения условно-диагностического уровня антител у детей до 6 лет при тифо-паратифозных заболеваниях в научной литературе не описаны.
и D, составляет для суммарных антител 1:100, для IgG 1:20 - 1:40. Значения условно-диагностического уровня антител у детей до 6 лет при тифо-паратифозных заболеваниях в научной литературе не описаны.
11.3. Для выявления предполагаемого источника инфекции при возникновении групповых и спорадических случаев шигеллеза и сальмонеллеза, вопрос об использовании серологического метода рекомендуется решать коллегиально, учитывая результаты эпидемиологического расследования очага, наличие клинических признаков заболевания и вакцинальный статус предполагаемого источника. В случае отрицательного результата бактериологического исследования пробы фекалий предполагаемого источника инфекции необходимо определять уровень антител класса IgG. При доследовании с диагностикумами шигеллезными (Зонне и Флекснера), сальмонеллезными комплексным или серогрупп А, В, C1, С2, D и Е диагностическим уровнем IgG следует считать 1:40 и выше (приложение к настоящим МР).
11.4. Для выявления источника инфекции при возникновении групповых и спорадических случаев брюшного тифа и паратифов диагностический уровень IgG составляет:
- при исследовании с О-диагностикумами 1:40 и выше;
- при доследовании с Ви-диагностикумом 1:40 и выше (источник - хронический бактерионоситель возбудителя брюшного тифа).
XII. Интерпретация результатов РПГА при исследовании парных сывороток
12.1. Для диагностики шигеллеза и сальмонеллеза, включая брюшной тиф и паратифы, сопоставляют уровни антител, обнаруженных в парных сыворотках, полученных в динамике заболевания с интервалом 7-8 дней: суммарных в нативной сыворотке и класса IgG в сыворотке, обработанной редуцентом. Парные сыворотки исследуют одновременно (в одном опыте), используя диагностикум одной серии: при определении суммарных антител и уточнении их класса.
12.2. Диагностически достоверным считается не менее чем четырехкратное (на 2 разведения) увеличение или снижение уровня специфических антител при исследовании парных сывороток. Уровень антител нарастает в течение первых двух недель болезни, на более поздних сроках снижается.
12.3. Интенсивность антителообразования зависит от возраста заболевшего и тяжести заболевания. При частом контакте с возбудителями и их антигенами у многих заболевших уровень антител в динамике заболевания увеличивается быстро - по типу вторичного иммунного ответа. Данная тенденция характерна для взрослых. Сроки и интервал взятия крови следующие:
- при подозрении на сальмонеллез и шигеллез: первая проба крови в остром периоде заболевания (не ранее 5-го дня от начала заболевания), вторая проба крови через 7-8 дней после первой;
- при подозрении на брюшной тиф и паратифы: первая проба крови после окончания лихорадочного периода, вторая проба крови через 7-8 дней после первой (в случае отрицательного результата бактериологического исследования и уровня антител в первой сыворотке ниже диагностического, п. 11.2).
При соблюдении сроков и интервалов взятия проб крови, как правило, выявляется достоверное нарастание уровня суммарных антител (IgM + IgG) и антител класса IgG. При нарушении сроков взятия крови изменения уровня антител могут быть менее выражены.
12.4. В результате серологического исследования возможно выявление нарастания уровня антител не к одному, а к двум и более взятым в реакцию антигенам, так как у грамотрицательных бактерий есть общие антигены, что приводит к появлению не только гомологических, но и гетерологических антител. Иммунологический ответ следует считать диагностическим (специфическим), если уровень антител к подозреваемому возбудителю увеличился в 4 и более раза, в то время как уровни гетерологических антител не изменились или снизились. Достоверным признаком инфекционного процесса является наличие диагностического уровня антител класса IgG в однократно взятой пробе (пункты 11.1, 11.2) и его нарастание при исследовании парных сывороток.
XIII. Особенности интерпретации результатов РПГА у детей
13.1. У детей первых месяцев жизни на фоне низкой иммунологической реактивности отсутствует или недостаточно напряжен гуморальный иммунитет. Проведение серологических исследований у детей в возрасте до 12 мес. не рекомендуется, поскольку обнаружить в РПГА специфические антитела к возбудителям ОКИ удается крайне редко. Наибольший процент положительных реакций отмечен у детей 6 лет и старше.
13.2. У детей в возрасте от 1 года до 6 лет уровень антител нарастает на 2-3-й неделях болезни и лишь у 60% обследованных достигает 1:100 и выше.
XIV. Интерпретация результатов РПГА при исследовании сыворотки, обработанной редуцентом
14.1. Если уровень антител после обработки редуцентом не снижается (результаты, полученные для обработанной и необработанной сыворотки одинаковы), то выявленные антитела относят к классу IgG, что свидетельствует о длительности заболевания более 7 дней.
14.2. Отсутствие антител в обработанной сыворотке достоверно свидетельствует об отсутствии антител класса IgG. Это косвенно указывает на принадлежность антител к классу IgM («ранние» антитела в первые дни заболевания). Сыворотку необходимо сохранить и повторно исследовать вместе с парной, взятой через 7-8 дней.
У хронических бактерионосителей, а также у реконвалесцентов и лиц, переболевших брюшным тифом, антитела класса IgM (свидетельствующие об остроте процесса) отсутствуют, поэтому результат (наличие антител в необработанной сыворотке и полное их исчезновение после обработки редуцентом) следует рассматривать как неспецифическую реакцию.
14.3. Снижение уровня антител в обработанной сыворотке по сравнению с необработанной свидетельствует о том, что антитела представлены классами IgM и IgG, снижение уровня произошло за счет разрушения IgM.
14.4. Увеличение уровня антител после обработки редуцентом указывает на лабораторную ошибку при постановке РПГА. Исследование следует повторить.
XV. Алгоритм серологического обследования при сальмонеллезе и шигеллезе
15.1. Для подтверждения клинического диагноза сальмонеллеза первоначально сыворотки изучают с комплексным диагностикумом эритроцитарным сальмонеллезным О-антигенным комплексным, содержащим антигены основных серологических групп (А, В, С, D, Е):
- при наличии положительного результата (выявлении диагностического уровня антител), сыворотка повторно исследуется в РПГА с диагностикумами эритроцитарными сальмонеллезными О-антигенными отдельных серологических групп (А, В, 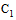 ,
, 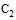 , D, Е);
, D, Е);
- если в сыворотке обнаружены антитела к сальмонеллезным О-антигенам 6, 7 (серогруппа 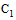 ) или 1, 9, 12 (cepoipynna D), то с учетом клинических или эпидемиологических показаний сыворотку дополнительно исследуют в РПГА с диагностикумом эритроцитарным сальмонеллезным Ви-антигенным для диагностики паратифа С или брюшного тифа.
) или 1, 9, 12 (cepoipynna D), то с учетом клинических или эпидемиологических показаний сыворотку дополнительно исследуют в РПГА с диагностикумом эритроцитарным сальмонеллезным Ви-антигенным для диагностики паратифа С или брюшного тифа.
15.2. Для подтверждения клинического диагноза шигеллеза, ввиду отсутствия комплексного диагностикума, сыворотки исследуют одновременно с тремя шигеллез- ными диагностикумами (Зонне, Флекснера 1-5; Флекснера 6).
15.3. Если уровень антител в сыворотке, взятой не ранее 5-го дня от начала заболевания, ниже диагностического уровня, сыворотку сохраняют в холодильнике и повторно исследуют одновременно со второй (парной) сывороткой, взятой через 7-8 дней после первой с диагностикумом той же серии.
15.4. Если в сыворотке выявлены антитела к антигенам Shigella или Salmonella в количестве, равном или превышающем условно-диагностический уровень, часть сыворотки обрабатывают редуцентом и повторно исследуют в РПГА для определения класса антител (одновременно исследуют обработанную редуцентом и необработанную пробы) (см. главу IX). При необходимости вторая часть необработанной сыворотки хранится в холодильнике для исследования с парной сывороткой, взятой через 7-8 дней после первой.
XVI. Алгоритм серологического обследования при брюшном тифе
16.1. Для подтверждения клинического диагноза брюшной тиф, в том числе ретроспективного (при позднем обращении больного за медицинской помощью, затяжном течении заболевания, когда существует высокая вероятность отрицательного результата бактериологического исследования (например, на фоне антибактериальной терапии) РПГА ставят с двумя диагностикумами эритроцитарными сальмонеллезными: О-антигенным серогруппы D (1, 9, 12) и Ви-антигенным.
16.2. В очаге брюшного тифа для активного выявления больных среди контактных лиц, относящихся к работникам отдельных профессий, производств и организаций, РПГА проводят с двумя диагностикумами эритроцитарными сальмонеллезными: О-антигенным серогруппы D (1, 9, 12) и Ви-антигенным.
16.3. Для выявления по эпидемическим показаниям предполагаемого источника инфекции (лица в состоянии хронического брюшнотифозного бактерионосительства, реконвалесценты или больные брюшным тифом в манифестной или субклинической форме) РПГА ставят с двумя диагностикумами эритроцитарными сальмонеллезными: О-антигенным серогруппы D (1, 9, 12) и Ви-антигенным.
16.4. При диспансерном наблюдении за лицами, переболевшими брюшным тифом, РПГА ставят с диагностикумом эритроцитарным сальмонеллезным Ви-антигенным.
16.5. Для выявления носителей возбудителя брюшного тифа среди работников отдельных профессий, производств и организаций при поступлении на работу проводят РПГА с диагностикумом эритроцитарным сальмонеллезным Ви-антигенным согласно санитарно-эпидемиологическим требованиям9.
16.6. Если в нативной сыворотке (взятой не ранее 7-го дня заболевания после окончания лихорадочного периода) уровень антител ниже условно-диагностического, сыворотку сохраняют в холодильнике при плюс 2 - плюс 8°С и повторно исследуют одновременно со второй (парной) сывороткой, взятой через 7-8 дней после первой с диагностикумом той же серии.
16.7. Если в нативной сыворотке уровень антител к антигенам возбудителя брюшного тифа или паратифов равен или превышает условно-диагностический, часть сыворотки обрабатывают редуцентом и повторно исследуют в РПГА для определения класса антител (одновременно исследуют обработанную редуцентом и необработанную пробы) (см. главу IX). При необходимости вторая часть необработанной сыворотки хранится в холодильнике для исследования с парной сывороткой, взятой через 7-8 дней после первой.
XVII. Особенности серологической диагностики состояния бактерионосительства
17.1. В случае формирования острого бактерионосительства (при брюшном тифе, паратифах, реже при других сальмонеллезах) характерно наличие в сыворотке высокого уровня антител класса IgG (уровень антител практически не снижается после обработки сыворотки редуцентом).
17.2. У хронических бактерионосителей возбудителя брюшного тифа уровень антител к сальмонеллезным О-антигенам может быть невысоким (1:50 - 1:100), но эти антитела представлены IgG. Уровень антител к Vi-антигену в большинстве случаев превышает 1 : 80, и они также представлены IgG.
17.3. У транзиторных бактерионосителей (не имеющих в анамнезе клинически выраженного заболевания) антитела к О- и Vi-антигенам возбудителей отсутствуют или представлены антителами класса IgM. Если после обработки сыворотки редуцентом уровень антител класса IgG сохраняется 1 : 40 и выше, то у таких пациентов можно предполагать наличие субклинической формы инфекции.
17.4. Повышение уровня антител класса IgG может происходить в результате многократной специфической вакцинации, поэтому при интерпретации результатов РПГА следует учитывать прививочный анамнез.
XVIII. Эффективность серологического метода диагностики ОКИ
18.1. При высоком уровне заболеваемости населения ОКИ, значительная часть которых остается этиологически нерасшифрованной, серологический метод является дополнительным методом для установления этиологии ОКИ. Полученные результаты оцениваются с учетом эпидемиологической обстановки, формы заболевания, сроков взятия сыворотки и т.д.
При проведении сероэпидемиологического анализа ОКИ серологическое исследование позволяет оценить число переболевших, интенсивность циркуляции возбудителя, риск заражения, пораженность отдельных социально-профессиональных групп населения.
При постановке РПГА макрометодом на 5-10-й день заболевания при острой дизентерии с выраженными клиническими проявлениями суммарные антитела выявляют у 70-80% больных (1:400 - 1:3200), при затяжном течении реже (30-40%) и невысокого уровня (1:100 - 1:400).
При сальмонеллезе с выраженными клиническими проявлениями диагностический уровень антител на 5-10-й день заболевания регистрируют у 80-90% больных (бактериологически подтвержденные случаи), выраженная динамика уровня антител отмечается только у 25-45% больных не ранее 2 3-й недели заболевания.
|
Руководитель Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека, Главный государственный санитарный врач Российской Федерации |
А.Ю. Попова |
------------------------------
1 СанПиН 3.3686-21 "Санитарно-эпидемиологические требования по профилактике инфекционных болезней", утвержденные постановлением Главного государственного санитарного врача Российской Федерации 28.01.2021 N 4 (зарегистрировано Минюстом 15.02.2021, регистрационный N 62500) (далее - СанПиН 3.3686-21).
2 МУ 4.2.2723-10 "Лабораторная диагностика сальмонеллезов, обнаружение сальмонелл в пищевых продуктах и объектах окружающей среды", утвержденные Роспотребнадзором 13.08.2010 (далее - МУ 4.2.2723-10); методические рекомендации "Бактериологическая диагностика брюшного тифа и паратифов А, В и С", утвержденные Роспотребнадзором 29.12.2007 N 0100/13745-07-34.
3 Примечание: допускается использование средств измерений, вспомогательного оборудования и материалов с аналогичными или лучшими характеристиками; допускается использование других реактивов с аналогичными характеристиками.
4 Утилизация отходов проводится в соответствии с СанПиН 3.3686-21.
5 Пункт 4 статья 38 Федерального закона от 21.11.2011 N 323-ФЗ "Об основах охраны здоровья граждан в Российской Федерации"; постановление Правительства Российской Федерации от 27.12.2012 N 1416 "Об утверждении Правил государственной регистрации медицинских изделий".
6 Статья 38 Федерального закона от 21.11.2011 № 323-Ф3 "Об основах охраны здоровья граждан в Российской Федерации".
7 МУ 4.2.2039-05 "Техника сбора и транспортирования биоматериалов в микробиологические лаборатории", утвержденные Роспотребнадзором 23.12.2005.
8 МУ 4.2.2723-10.
9 СанПиН 3.3686-21.
------------------------------
Приложение
к МР 4.2.0249-21
Понятие «условно-диагностический уровень антител»
1. На величину «диагностического» уровня антител влияет конкретная эпидемиологическая ситуация на территории, на которой риск заражения возбудителями шигеллеза, сальмонеллеза, брюшного тифа и степень их распространения среди населения варьируют, что ведет к уменьшению или повышению уровня «фоновых» антител у здоровых лиц. Рекомендуется установление «диагностического» уровня в каждом конкретном регионе (административной территории) по результатам титрования сывороток, взятых не менее чем от 100 здоровых лиц (взрослого и детского контингента).
2. Значение «диагностического» уровня в определенной степени условно и зависит от многих факторов. В условиях многолетней циркуляции возбудителей среди людей, контаминации ими пищевых продуктов и объектов окружающей бреды, при естественном инфицировании населения небольшими дозами возбудителей в сыворотках здоровых людей присутствуют анамнестические антитела (так называемые «фоновые» антитела) классов IgM и IgG.
3. Определенный уровень антител в сыворотках здоровых людей может быть обусловлен:
- перенесенным в прошлом заболеванием, в том числе в стертой или субклинической форме (шигеллез, сальмонеллез, брюшной тиф);
- иммунным ответом на вакцинацию (брюшной тиф, шигеллез Зонне), о чем свидетельствует сертификат профилактических прививок или справка из автоматической системы управления иммунизацией.
Библиографические ссылки
1. Федеральный закон от 30.03.1999 № 52-ФЗ «О санитарно-эпидемиологическом благополучии населения».
2. Федеральный закон от 21.11.2011 № 323-Ф3 «Об основах охраны здоровья граждан в Российской Федерации».
3. Постановление Правительства Российской Федерации от 27.12.2012 № 1416 «Об утверждении Правил государственной регистрации медицинских изделий».
4. СанПиН 3.3686-21 «Санитарно-эпидемиологические требования по профилактике инфекционных болезней».
5. МУ 4.2.2039-05 «Техника сбора и транспортирования биоматериалов в микробиологические лаборатории».
6. МУ 4.2.2723-10 «Лабораторная диагностика сальмонеллезов, обнаружение сальмонелл в пищевых продуктах и объектах окружающей среды».
7. Методические рекомендации № 0100/13745-07-34 «Бактериологическая диагностика брюшного тифа и паратифов А, В и С».
Обзор документа
С 1 сентября 2021 г. применяются Методические рекомендации МР 4.2.0249-21 "Серологическая диагностика острых кишечных инфекций методом РПГА (шигеллеза, сальмонеллеза и брюшного тифа)".
Рекомендации предназначены для органов и организаций Роспотребнадзора, а также могут быть использованы научными и медицинскими организациями, осуществляющими серологическую диагностику острых кишечных инфекций.



(1).jpg)


