Письмо Федеральной службы по надзору в сфере здравоохранения от 9 февраля 2016 г. N 01И-218/16 "Об отзыве декларации о соответствии"
Федеральная служба по надзору в сфере здравоохранения сообщает о принятом решении АО "Химико-фармацевтический комбинат "АКРИХИН" отозвать декларацию о соответствии N РОСС РL.ФВ14.Д11996 от 03.08.2015 на лекарственный препарат "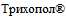 , таблетки 250 мг 10 шт., блистеры (2), пачки картонные" серии 40415 производства Фармацевтический завод "Польфарма А.О." (Польша), в связи с его несоответствием требованиям нормативной документации по показателю "Описание".
, таблетки 250 мг 10 шт., блистеры (2), пачки картонные" серии 40415 производства Фармацевтический завод "Польфарма А.О." (Польша), в связи с его несоответствием требованиям нормативной документации по показателю "Описание".
О приостановлении реализации указанной серии лекарственного препарата субъекты обращения лекарственных средств информированы письмом Росздравнадзора от 29.10.2015 N 01И-1851/15.
Росздравнадзор предлагает АО "Химико-фармацевтический комбинат "АКРИХИН" предоставить сведения об изъятии из обращения данной серии лекарственного препарата, выпущенной в гражданский оборот на основании указанной декларации о соответствии.
Федеральная служба по надзору в сфере здравоохранения предлагает субъектам обращения лекарственных средств предоставить в территориальный орган Росздравнадзора сведения, подтверждающие изъятие из обращения указанной серии лекарственного препарата, выпущенной в гражданский оборот на основании данной декларации о соответствии.
Территориальным органам Росздравнадзора обеспечить контроль за выявлением и изъятием данной серии лекарственного препарата, выпущенной в гражданский оборот на основании указанной декларации о соответствии. О проведенной работе информировать Росздравнадзор.
| М.А. Мурашко |
Обзор документа
АО "Химико-фармацевтический комбинат "АКРИХИН" принял решение отозвать декларацию о соответствии N РОСС РL.ФВ14.Д11996 от 03.08.2015 на лекарственный препарат "Трихопол" 250 мг серии 40415 производства Фармацевтический завод "Польфарма А.О." (Польша). Решение принято в связи с его несоответствием требованиям НД по показателю "Описание".
АО "Химико-фармацевтический комбинат "АКРИХИН" следует предоставить сведения об изъятии из обращения данной серии препарата, сопровождающейся указанной декларацией о соответствии.
Субъектам обращения лекарственных средств предлагается проверить наличие указанной серии препарата, и представить информацию о ее изъятии в территориальный орган Росздравнадзора.



(1).jpg)


