Письмо Федеральной службы по надзору в сфере здравоохранения от 30 декабря 2015 г. N 01И-2377/15 "О поступлении информации о выявлении недоброкачественных лекарственных препаратов"
Федеральная служба по надзору в сфере здравоохранения сообщает о поступлении информации о выявлении лекарственных препаратов, качество которых не отвечает установленным требованиям:
1. Забракованные ОГУ "Центр контроля качества и сертификации лекарственных средств" (Липецкая область):
- 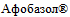 , таблетки 10 мг 20 шт., упаковки ячейковые контурные (3), пачки картонные, производства ОАО "Фармстандарт-Лексредства", Россия, владелец ООО "ЮНИКОМ", Липецкая область/поставщик АО НПК "Катрен", Воронежская область, показатель "Упаковка" (в части контурных ячейковых упаковках отсутствуют таблетки) - серии 940315.
, таблетки 10 мг 20 шт., упаковки ячейковые контурные (3), пачки картонные, производства ОАО "Фармстандарт-Лексредства", Россия, владелец ООО "ЮНИКОМ", Липецкая область/поставщик АО НПК "Катрен", Воронежская область, показатель "Упаковка" (в части контурных ячейковых упаковках отсутствуют таблетки) - серии 940315.
2. Забракованные ГБУЗ Кемеровской области "Центр контроля качества и сертификации лекарственных средств":
- Кальция глюконат-Виал, раствор для внутривенного и внутримышечного введения 100 мг/мл 10 мл, ампулы (10), упаковки ячейковые контурные (1), пачки картонные, производства "Северная Китайская Фармацевтическая Корпорация Лтд", Китай, владелец ООО "Сити-Маркет", г. Томск, Томская область, показатель "Описание" (в одной ампуле жидкость с осадком белого цвета) - серии 140405.
3. Забракованные ГБУЗ Республики Мордовия "Мордовский республиканский центр контроля качества и сертификации лекарственных средств":
- Аспаркам-Фармак, раствор для внутривенного введения 10 мл, ампулы (5), упаковки ячейковые контурные (2), пачки картонные, производства ОАО "Фармак", Украина, владелец ГБУЗ Республики Мордовия "Республиканская клиническая больница N 5", г. Саранск, Республика Мордовия, показатель "Описание" (в части ампул обнаружены кристаллы) - серии 80114.
Территориальным органам Росздравнадзора по Воронежской, Липецкой и Томской областям, Республике Мордовия обеспечить контроль за изъятием из обращения и уничтожением в установленном порядке указанных партий недоброкачественных лекарственных препаратов.
Федеральная служба по надзору в сфере здравоохранения сообщает о приостановлении реализации иных партий вышеуказанных серий лекарственных препаратов.
Росздравнадзор предлагает субъектам обращения лекарственных средств, медицинским организациям провести проверку наличия указанных серий лекарственных препаратов, о результатах которой информировать территориальный орган Росздравнадзора.
Территориальным органам Росздравнадзора обеспечить контроль за выявлением и изъятием из обращения указанной серии лекарственного препарата. О проведенной работе информировать Росздравнадзор.
Федеральная служба по надзору в сфере здравоохранения указывает изготовителям (продавцам, лицам, выполняющим функции иностранного изготовителя) указанных серий лекарственных препаратов на необходимость проведения мероприятий, предусмотренных статьей 38 Федерального закона от 27.12.2002 N 184-ФЗ "О техническом регулировании".
Росздравнадзор предписывает изготовителям (продавцам, лицам, выполняющим функции иностранного изготовителя) в течение десяти дней с момента получения данного письма представить сведения о проведенной работе, включая материалы проверки достоверности информации и программу мероприятий по предотвращению причинения вреда, на адрес: control_ls@roszdravnadzor.ru с последующей досылкой на бумажном носителе.
Федеральная служба по надзору в сфере здравоохранения обращает внимание, что непредставление или несвоевременное представление, либо представление заведомо недостоверных сведений в Росздравнадзор, а также невыполнение в установленный срок предписания, решения Росздравнадзора влечет ответственность, предусмотренную соответственно ст. 19.7.8. и ч. 21 ст. 19.5 Кодекса Российской Федерации об административных правонарушениях.
| М.А. Мурашко |
Обзор документа
Сообщается о выявлении лекарственных препаратов, качество которых не отвечает установленным требованиям.
Это - "Афобазол" 10 мг серии 940315, производства ОАО "Фармстандарт-Лексредства" (Россия), показатель "Упаковка" (в части контурных ячейковых упаковках отсутствуют таблетки), "Кальция глюконат-Виал" 100 мг/мл серии 140405, производства "Северная Китайская Фармацевтическая Корпорация Лтд" (Китай), показатель "Описание" (в одной ампуле жидкость с осадком белого цвета), "Аспаркам-Фармак" 10 мл серии 80114, производства ОАО "Фармак" (Украина), показатель "Описание" (в части ампул обнаружены кристаллы).
Приостанавливается реализация иных партий вышеуказанных серий лекарств.
Субъектам обращения лекарственных средств и медицинским организациям предлагается проверить наличие указанных серий препаратов. О результатах информировать территориальный орган Росздравнадзора.



(1).jpg)


