Информация Министерства здравоохранения РФ "Порядок работы с маркированными лекарственными препаратами в обособленных подразделениях медицинских организаций (амбулаториях, фельдшерских и фельдшерско-акушерских пунктах, центрах (отделениях) общей врачебной (семейной) практики) (далее - обособленные подразделения медицинских организаций)"
Общие положения
| Любые физические действия, осуществляемые с лекарственными препаратами субъектами обращения лекарственных средств на всех этапах товаропроводящей цепи, должны быть отражены в государственной информационной системе мониторинга движения лекарственных препаратов для медицинского применения (далее - ФГИС МДЛП) |
|---|
Перемещение лекарственных препаратов в рамках гражданско-правовых отношений от одного субъекта обращения лекарственных средств к другому субъекту обращения лекарственных средств сопровождается передачей сведений в ФГИС МДЛП с использованием одного из следующих вариантов порядка предоставления сведений:
- прямой порядок представления сведений (прямой акцепт), при котором в ФГИС МДЛП отправителем регистрируются сведения об отгрузке покупателю лекарственных препаратов, а получателем осуществляется подтверждение в ФГИС МДЛП зарегистрированных отправителем сведений об отгрузке лекарственных препаратов.
- обратный порядок предоставления сведений (обратный акцепт), при котором в ФГИС МДЛП получателем регистрируются сведения о приемке лекарственных препаратов на склад, а отправителем осуществляется подтверждение сведений о приемке на склад покупателя.
Решение о выборе порядка предоставления сведений принимается субъектами обращения лекарственных средств, предоставляющими такие сведения, самостоятельно.
Сведения, передаваемые в ФГИС МДЛП, формируются субъектом обращения лекарственных средств вручную или автоматическим способом с использованием товароучетных систем участников, интегрированных с ФГИС МДЛП, и предоставляются в форме электронных документов (файлов) в формате xml. Составление xml-документов, необходимых для осуществления информационного обмена с ФГИС МДЛП, осуществляется на основании соответствующих схем логической модели обмена файлов ФГИС МДЛП, описание которой приведено на сайте честныйзнак.рф в разделе "Документы для работы в МДЛП".
Для работы с ФГИС МДЛП в автоматическом режиме рабочие места сотрудников, ответственных за приемку и отпуск маркированных лекарственных препаратов, должны быть оборудованы 2D-сканером штрих-кодов (для приемки и розничной торговли лекарственными препаратами) и регистраторами выбытия (для вывода из оборота лекарственных препаратов в рамках отпуска бесплатно по льготному рецепту или для оказания медицинской помощи).
2D-сканер представляет собой устройство для получения информации из линейных и матричных штриховых кодов с выбором технологии распознавания и особенностей декодирования в зависимости от типа штрих-кода. 2D-сканер приобретается субъектом обращения лекарственных средств самостоятельно. Перечень протестированных устройств размещен в разделе "Проверка сканера" на сайте честныйзнак.рф. При наличии у участника оборота 2D-сканера необходимо проверить его работоспособность на предмет корректного считывания кода маркировки. Соответствующая инструкция размещена в разделе "Проверка сканера" на сайте честныйзнак.рф.
Регистратор выбытия представляет собой устройство, осуществляющее считывание кода маркировки DataMatrix, формирование данных о лекарственных препаратах и последующую передачу в ФГИС МДЛП информации о фиксации факта выбытия упаковки лекарственного препарата из оборота. Устройство имеет программный интерфейс, позволяющий передавать сведения о выбытии лекарственного препарата как в автономном, так и в сетевом режиме. Подробная информация о режимах работы и способах подключения регистраторов выбытия приведена на сайте честныйзнак.рф в разделе "Регистраторы выбытия". В целях автоматизации процесса передачи данных при выводе из оборота лекарственных препаратов субъекту обращения лекарственных препаратов рекомендуется интегрировать регистратор выбытия с используемой им товароучетной системой. Интеграция выполняется субъектом обращения лекарственных средств самостоятельно либо с привлечением поставщика ИТ-услуг. При разработке интеграционного взаимодействия необходимо руководствоваться технической документацией, размещенной на сайте честныйзнак.рф в разделе "Выдержка из технической спецификации на поставку регистратора выбытия".
Оснащение обособленных подразделений медицинских организаций регистраторами выбытия происходит на основании заявок, подготовленных и направленных в адрес оператора системы мониторинга ООО "Оператор-ЦРПТ" головными медицинскими организациями. Регистратор выбытия предоставляется оператором системы мониторинга на безвозмездной основе на основании договора по представлению регистратора выбытия лекарственных препаратов субъектам обращения лекарственных средств, форма которого утверждена приказом Минпромторга России от 13.08.2019 N 2973. Подробности о заказе, условиях и сроках установления регистратора выбытия приведены на сайте честныйзнак.рф, в разделе инструкций для медицинской организации.
| Важно! Регистратор выбытия не используется при осуществлении розничной торговли лекарственными препаратами |
|---|
1. Обособленные подразделения медицинских организаций, обеспеченные доступом к информационно-коммуникационной сети "Интернет" (Рисунок 1)
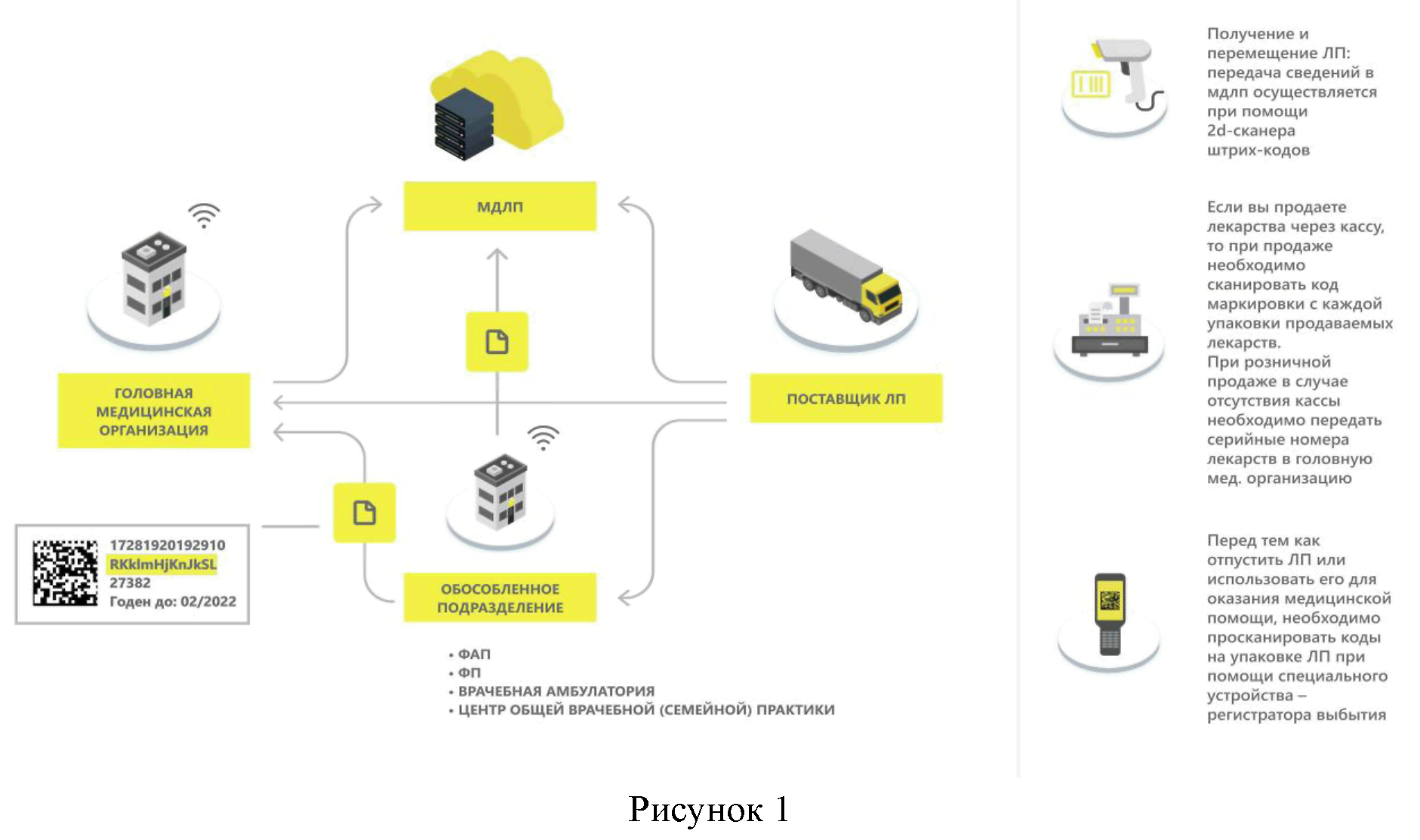
Приказом Минздрава России от 03.12.2019 N 984н внесены изменения в стандарт оснащения врачебной амбулатории, фельдшерско-акушерского пункта, фельдшерского здравпункта, предусматривающие наличие в них не менее одного рабочего места врача (фельдшера) с персональным компьютером и выходом в информационно-телекоммуникационную сеть "Интернет"
1) Приемка маркированных лекарственных препаратов
В зависимости от условий поставки, указанных в договоре между головной медицинской организацией и поставщиком лекарственных препаратов, приемка лекарственных препаратов может быть осуществлена как головной медицинской организацией с последующим перемещением необходимых лекарственных препаратов в обособленные подразделения, так и непосредственно обособленными подразделениями головной медицинской организации.
В случае осуществления приемки лекарственных препаратов головной медицинской организацией ответственные сотрудники указанной медицинской организации вносят в ФГИС МДЛП сведения о принятом товаре по схеме 701 (в случае прямого акцепта) или схеме 416 (в случае обратного акцепта) с указанием идентификатора места осуществления деятельности головной медицинской организации. При перемещении лекарственных препаратов из головной медицинской организации в ее обособленные подразделения ответственные сотрудники головной медицинской организации направляют в ФГИС МДЛП сведения о перемещении лекарственных препаратов между различными адресами осуществления деятельности по схеме 431. Участие сотрудников обособленных подразделений медицинской организации в передаче сведений о приемке лекарственных препаратов не требуется.
В случае осуществления поставки лекарственных препаратов непосредственно в обособленные подразделения медицинской организации, минуя головную медицинскую организацию, сведения о приемке лекарственных препаратов в ФГИС МДЛП направляются ответственным сотрудником обособленного подразделения медицинской организации по схеме 701 (в случае прямого акцепта) или схеме 416 (в случае обратного акцепта) с обязательным указанием в хml-документе идентификатора места осуществления деятельности обособленного подразделения медицинской организации.
В случае поставки лекарственных препаратов, предназначенных для последующей реализации обособленными подразделениями, расположенными в сельских поселениях, в которых отсутствуют аптечные организации, по договору комиссии, сведения о приемке лекарственных препаратов вносятся в ФГИС МДЛП ответственными сотрудниками головной медицинской организации (в случае поставки в головную медицинскую организацию) или ответственным сотрудником обособленного подразделения медицинской организации (в случае поставки непосредственно в обособленное подразделение) с использованием схемы 701 с обязательным указанием в хml-документе идентификатора места осуществления деятельности головной медицинской организации или идентификатора места осуществления деятельности обособленного подразделения медицинской организации, соответственно.
Убедившись в том, что поставленные лекарственные препараты находятся по данным ФГИС МДЛП на балансе головной медицинской организации или обособленного подразделения медицинской организации, ответственные сотрудники указанной медицинской организации или обособленного подразделения вносят в ФГИС МДЛП сведения о расформировании поступившей транспортной упаковки, содержащей лекарственные препараты, по схеме 912 или сведения об изъятии из транспортной упаковки вторичных упаковок лекарственных препаратов по схеме 913 для обеспечения дальнейшего вывода из оборота каждой единицы товара. При наличии нескольких уровней вложенности упаковок лекарственных препаратов в транспортную упаковку изъятие вторичных упаковок лекарственных препаратов из транспортной упаковки необходимо осуществлять от вышестоящего уровня к нижестоящему, отражая операцию для каждого из уровней в ФГИС МДЛП.
Срок подачи сведений в ФГИС МДЛП о приемке лекарственных препаратов, сведений о перемещении лекарственных препаратов между местами осуществления деятельности, сведений о расформировании поступившей транспортной упаковки и сведений об изъятии из транспортной упаковки вторичных упаковок лекарственных препаратов - до 5 рабочих дней.
2) Вывод из оборота маркированных лекарственных препаратов при оказании медицинской помощи
Вывод из оборота лекарственных препаратов при оказании медицинской помощи в обособленных подразделениях медицинской организации, обеспеченных доступом к информационно-телекоммуникационной сети "Интернет", осуществляется с использованием устройств регистрации выбытия.
Для вывода из оборота лекарственных препаратов при оказании медицинской помощи ответственному сотруднику обособленного подразделения необходимо отсканировать код маркировки DataMatrix, нанесенный на упаковку лекарственного препарата. При успешном распознавании кода маркировки на экране регистратора выбытия появится наименование лекарственного препарата. В случае использования товароучетной системы, интегрированной с ФГИС МДЛП и регистратором выбытия, информация о лекарственном препарате и о том, может ли данный препарат быть выведен из оборота, появится на экране компьютера. Для завершения процесса вывода из оборота лекарственных препаратов с помощью программного интерфейса регистратора выбытия следует выполнить действие "Зарегистрировать выбытие". Информация о выводе из оборота будет направлена в ФГИС МДЛП в автоматическом режиме посредством функционала регистратора выбытия (схема 10531).
Срок подачи сведений в ФГИС МДЛП о выводе из оборота лекарственных препаратов при оказании медицинской помощи - до 5 рабочих дней.
3) Вывод из оборота маркированных лекарственных препаратов при отпуске бесплатно по рецепту на лекарственный препарат
Вывод из оборота лекарственных препаратов при отпуске бесплатно по рецепту на лекарственный препарат обособленными подразделениями медицинских организаций, обеспеченными доступом к информационно-телекоммуникационной сети "Интернет" и расположенными в сельских поселениях, в которых отсутствуют аптечные организации, осуществляется с использованием устройств регистрации выбытия.
Для вывода из оборота лекарственных препаратов при отпуске бесплатно по рецепту на лекарственный препарат ответственному сотруднику обособленного подразделения необходимо отсканировать код маркировки DataMatrix, нанесенный на упаковку лекарственного препарата. При успешном распознавании кода маркировки на экране регистратора выбытия появится наименование лекарственного препарата. В случае использования товароучетной системы, интегрированной с ФГИС МДЛП и регистратором выбытия, информация о лекарственном препарате и о том, может ли данный препарат быть выведен из оборота, появится на экране компьютера. Для завершения процесса вывода из оборота лекарственного препарата необходимо ввести на регистраторе выбытия или в товароучетной системе реквизиты рецепта (дата, серия и номер) и с помощью программного интерфейса регистратора выбытия выполнить действие "Зарегистрировать выбытие". Информация о выводе из оборота будет направлена в ФГИС МДЛП в автоматическом режиме посредством функционала регистратора выбытия (схема 10521).
Срок подачи сведений в ФГИС МДЛП о выводе из оборота лекарственных препаратов при отпуске бесплатно по рецепту на лекарственный препарат - до 5 рабочих дней.
4) Вывод из оборота маркированных лекарственных препаратов при осуществлении розничной торговли лекарственными препаратами, в том числе отпуск лекарственных препаратов со скидкой по рецепту на лекарственные препараты
Передача сведений в ФГИС МДЛП о выведенных из оборота лекарственных препаратов при осуществлении розничной торговли лекарственными препаратами, в том числе отпуске лекарственных препаратов со скидкой по рецепту на лекарственные препараты, обособленными подразделениями медицинских организаций, расположенными в сельских поселениях, в которых отсутствуют аптечные организации, может быть осуществлена одним из следующих способов.
В случае использования обособленными подразделениями медицинской организации контрольно-кассовой техники сведения о реализованных лекарственных препаратах (отпущенных со скидкой по рецепту на лекарственные препараты) передаются обособленным подразделением медицинской организации в ФГИС МДЛП через оператора фискальных данных в режиме реального времени (схема 10511).
Если обособленными подразделениями медицинских организаций, расположенными в сельских поселениях, в которых отсутствуют аптечные организации, контрольно-кассовая техника в соответствии с Федеральным законом "О применении контрольно-кассовой техники при осуществлении расчетов в Российской Федерации" от 22.05.2003 N 54-ФЗ не применяется, то передача сведений о реализованных лекарственных препаратах (отпущенных со скидкой по рецепту на лекарственные препараты) в ФГИС МДЛП осуществляется ответственными сотрудниками головной медицинской организации. Сообщения о выводе из оборота лекарственных препаратов формируются с использованием функционала ФГИС МДЛП по схеме 511 на основании отчетности обособленного подразделения медицинской организации о реализации лекарственных препаратов, содержащей информацию о серийных номерах проданных упаковок лекарственных препаратов, с обязательным указанием в хml-документе идентификатора места деятельности обособленного подразделения медицинской организации.
Срок подачи сведений в ФГИС МДЛП о выводе из оборота лекарственных препаратов при осуществлении розничной торговли, в том числе отпуске лекарственных препаратов со скидкой по рецепту на лекарственный препарат - до 5 рабочих дней.
2. Обособленные подразделения медицинских организаций, не обеспеченные доступом к информационно-коммуникационной сети "Интернет" (Рисунок 2)
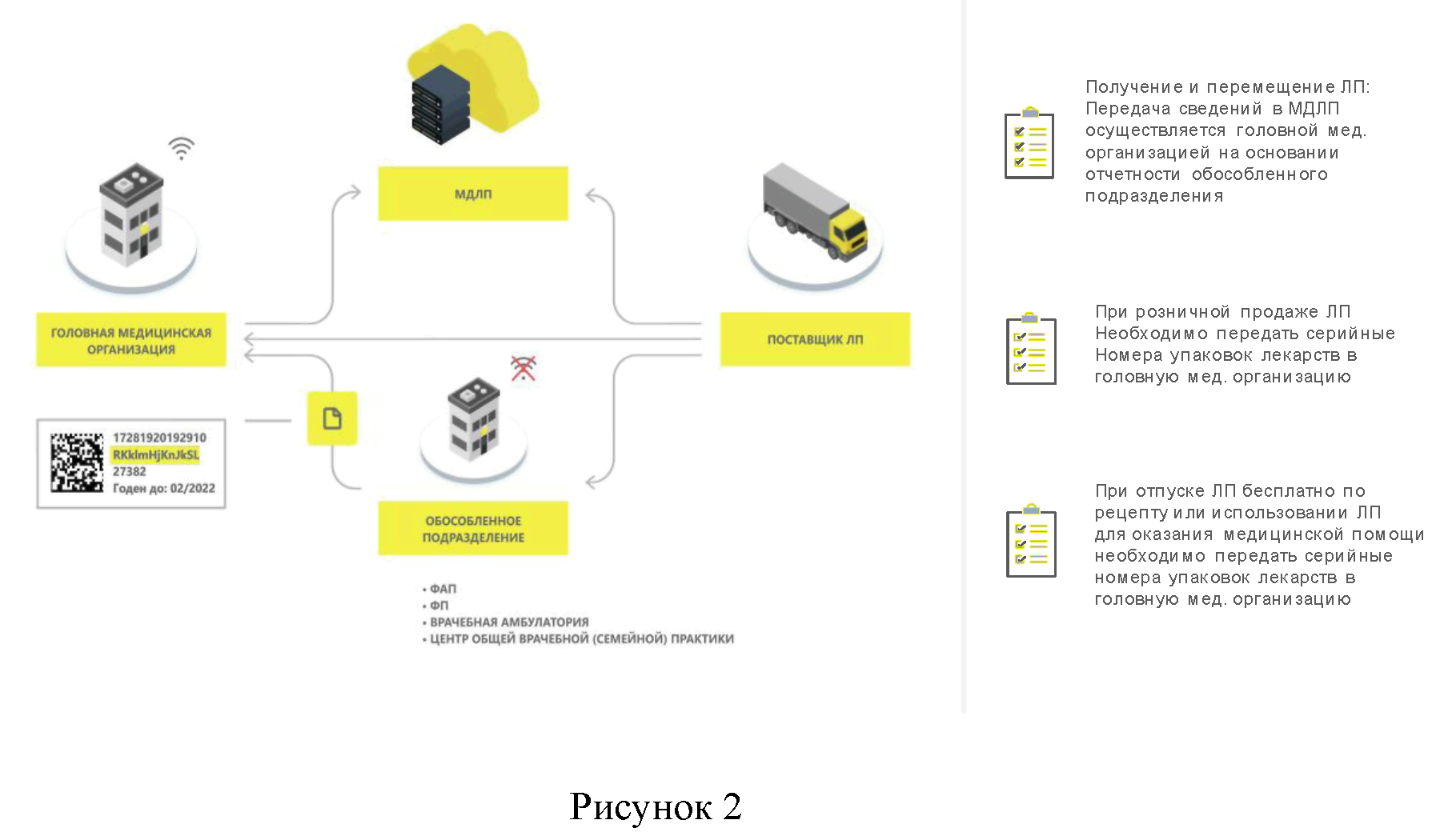
1) Приемка маркированных лекарственных препаратов
В зависимости от условий поставки, указанных в договоре между головной медицинской организацией и поставщиком лекарственных препаратов, приемка лекарственных препаратов может быть осуществлена как головной медицинской организацией с последующим перемещением необходимых лекарственных препаратов в обособленные подразделения, так и непосредственно обособленными подразделениями головной медицинской организации.
В случае осуществления приемки лекарственных препаратов головной медицинской организацией ответственные сотрудники указанной медицинской организации вносят в ФГИС МДЛП сведения о принятом товаре по схеме 701 (в случае прямого акцепта) или схеме 416 (в случае обратного акцепта) с указанием идентификатора места осуществления деятельности головной медицинской организации. При перемещении лекарственных препаратов из головной медицинской организации в ее обособленные подразделения ответственные сотрудники головной медицинской организации направляют в ФГИС МДЛП сведения о перемещении лекарственных препаратов между различными адресами осуществления деятельности по схеме 431. Участие сотрудников обособленных подразделений медицинской организации в передаче сведений о приемке лекарственных препаратов не требуется.
В случае осуществления поставки лекарственных препаратов непосредственно в обособленные подразделения медицинской организации, минуя головную медицинскую организацию, сведения о приемке лекарственных препаратов в ФГИС МДЛП направляются ответственными сотрудниками головной медицинской организации. Сообщения формируются с использованием функционала ФГИС МДЛП по схеме 701 (в случае прямого акцепта) или схеме 416 (в случае обратного акцепта) на основании отчетности обособленного подразделения медицинской организации, содержащей информацию о серийных номерах упаковок поставленных лекарственных препаратов, с обязательным указанием в хml-документе идентификатора места осуществления деятельности обособленного подразделения медицинской организации.
В случае поставки лекарственных препаратов, предназначенных для последующей реализации обособленными подразделениями, расположенными в сельских поселениях, в которых отсутствуют аптечные организации, по договору комиссии, сведения о приемке лекарственных препаратов вносятся в ФГИС МДЛП ответственными сотрудниками головной медицинской организации в вышеуказанном порядке.
Убедившись в том, что поставленные лекарственные препараты находятся по данным ФГИС МДЛП на балансе головной медицинской организации или обособленного подразделения медицинской организации, ответственные сотрудники указанной медицинской организации вносят в ФГИС МДЛП сведения о расформировании поступившей транспортной упаковки, содержащей лекарственные препараты, по схеме 912 или сведения об изъятии из транспортной упаковки вторичных упаковок лекарственных препаратов по схеме 913 для обеспечения дальнейшего вывода из оборота каждой единицы товара. При наличии нескольких уровней вложенности упаковок лекарственных препаратов в транспортную упаковку изъятие вторичных упаковок лекарственных препаратов из транспортной упаковки необходимо осуществлять от вышестоящего уровня к нижестоящему, отражая операцию для каждого из уровней в ФГИС МДЛП.
Срок подачи сведений в ФГИС МДЛП о приемке лекарственных препаратов, сведений о перемещении лекарственных препаратов между местами осуществления деятельности, сведений о расформировании поступившей транспортной упаковки и сведений об изъятии из транспортной упаковки вторичных упаковок лекарственных препаратов - до 5 рабочих дней.
2) Вывод из оборота маркированных лекарственных препаратов при оказании медицинской помощи
Передача сведений о лекарственных препаратах, выведенных из оборота обособленными подразделениями медицинской организации, не обеспеченными доступом к информационно-телекоммуникационной сети "Интернет", при оказании медицинской помощи, в ФГИС МДЛП осуществляется ответственными сотрудниками головной медицинской организации. Сообщения формируются с использованием функционала ФГИС МДЛП по схеме 531 на основании отчетности обособленного подразделения медицинской организации, содержащей информацию о серийных номерах упаковок лекарственных препаратов, использованных при оказании медицинской помощи, с обязательным указанием в хml-документе идентификатора места деятельности обособленного подразделения медицинской организации.
Срок подачи сведений в ФГИС МДЛП о выводе из оборота лекарственных препаратов при оказании медицинской помощи - до 5 рабочих дней.
3) Вывод из оборота маркированных лекарственных препаратов при отпуске бесплатно по рецепту на лекарственный препарат
Передача сведений о лекарственных препаратах, выведенных из оборота обособленными подразделениями медицинской организации, не обеспеченными доступом к информационно-телекоммуникационной сети "Интернет", при отпуске бесплатно по рецепту на лекарственный препарат, в ФГИС МДЛП осуществляется ответственными сотрудниками головной медицинской организации. Сообщения формируются с использованием функционала ФГИС МДЛП по схеме 521 на основании отчетности обособленного подразделения медицинской организации, содержащей информацию о серийных номерах упаковок лекарственных препаратов, отпущенных бесплатно по рецепту, с обязательным указанием в хml-документе идентификатора места деятельности обособленного подразделения медицинской организации.
Срок подачи сведений в ФГИС МДЛП о выводе из оборота лекарственных препаратов при отпуске бесплатно по рецепту на лекарственный препарат - до 5 рабочих дней.
4) Вывод из оборота маркированных лекарственных препаратов при осуществлении розничной торговли лекарственными препаратами, в том числе отпуск лекарственных препаратов со скидкой по рецепту на лекарственные препараты
Передача сведений о лекарственных препаратах, выведенных из оборота обособленными подразделениями медицинской организации, не обеспеченными доступом к информационно-телекоммуникационной сети "Интернет", при осуществлении розничной торговли, в том числе отпуске лекарственных препаратов со скидкой по рецепту на лекарственный препарат, в ФГИС МДЛП осуществляется ответственными сотрудниками головной медицинской организации. Сообщения формируются с использованием функционала ФГИС МДЛП по схеме 511 на основании отчетности обособленного подразделения медицинской организации, содержащей информацию о серийных номерах реализованных (отпущенных со скидкой по рецепту) упаковок лекарственных препаратов, с обязательным указанием в хml-документе идентификатора места деятельности обособленного подразделения медицинской организации.
Срок подачи сведений в ФГИС МДЛП о выводе из оборота лекарственных препаратов при осуществлении розничной торговли, в том числе отпуске лекарственных препаратов со скидкой по рецепту на лекарственный препарат - до 5 рабочих дней.
Обзор документа
Минздрав разъяснил порядок работы с маркированными лекарственными препаратами в амбулаториях, фельдшерских и фельдшерско-акушерских пунктах и центрах (отделениях) общей врачебной (семейной) практики. Указаны сроки совершения отдельных процедур и способы направления требуемых сведений.
Отмечено, что любые физические действия, которые совершают субъекты обращения лекарств на всех этапах товаропроводящей цепи, должны быть отражены в государственной информационной системе мониторинга движения лекарственных препаратов для медицинского применения (ФГИС МДЛП).



(1).jpg)


